(10分,每空2分)现有浓度均为0.1 mol/L的下列溶液:①醋酸、②硫酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦硫酸铵,⑧氨水,请回答下列问题:
(1)①②③④四种溶液中由水电离出的H+浓度由小到大的顺序是(填序号)__________________。
(2)④⑤⑥⑦⑧五种溶液中NH4+浓度由小到大的顺序是(填序号)__________________ 。
(3)将③和④等体积混合后,混合液中各离子浓度由小到大的顺序是__________________。
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”)__________________25℃。在t℃时将pH=2的H2SO4的溶液a L与pH=11的NaOH溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=___________ 。
(1)①pH= a的CH3COOH溶液稀释100倍后所得溶液pHa +2(填“>”或“<”)
②0.01mol/LCH3COOH溶液的pH2(填“>”或“<”);
③0.1mol/LCH3COONa溶液的pH7(填“>”或“<”);
(2)某固体是由Na2CO3、NaOH、MgCl2、AlCl3、BaCl2、Fe2(SO4)3和(NH4)2SO4中的两种混合而成。取该固体溶于水得到无色澄清溶液,向该溶液中加入稀硫酸,有白色沉淀生成,继续加入稀硫酸,沉淀又完全消失,且整个过程中无气体产生。则 原固体中含有物质有和 。(写化学式)
求下列混合后溶液的pH:(lg2=0.3 lg5=0.7)
(1)把pH=2和pH=4的两种强酸溶液等体积混合,其pH=_______。
(2)把pH=12和pH=14的两种强碱溶液等体积混合,其pH=_________。
(3)把pH=2的H2SO4溶液和pH=10的NaOH溶液等体积混合,其pH=_______。
按要求完成下列化学反应式
(1)硫酸氢钠在水溶液中的电离方程式 ;
(2)Na2CO3溶液水解的离子方程式 ;
(3)Al2(SO4)3溶液与NaHCO3溶液混合反应的离子方程式 ;
(4)Mg3N2与水反应的化学方程式 ;
将一定质量的Mg和Al的混合物投入2.0 mol/L,250 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入一定浓度的NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。回答下列问题:
(1)由图可知加入镁的物质的量是 _____________________。
(2)当加入NaOH溶液的体积小于20mL时发生的离子反应是__________,当加入NaOH溶液的体积大于200 mL时发生的离子反应是______________。
(3)NaOH溶液的物质的量浓度为______________________。
如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题: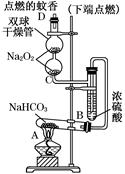
(1)在A试管内发生反应的化学方程式是___________________。
(2)B装置的作用是__________________________________。
(3)在双球干燥管内发生反应的化学方程式为_______________。
(4)双球干燥管内观察到的实验现象是__________________________
____________________________________________________________________。
上述实验现象说明________________________________________________________。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是_________。