工业上用CO生产甲醇的反应为CO(g)+2H2(g)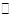 CH3OH(g)。图10表示反应中能量的变化;图11表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图。下列叙述错误的是
CH3OH(g)。图10表示反应中能量的变化;图11表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图。下列叙述错误的是

图10 图11 图12
| A.CO和H2合成CH3OH的反应:△H<0,△S>0 |
| B.保持温度不变,再充入1molCO和2molH2,反应达到新平衡时n(CH3OH)/n(CO)减小 |
| C.图10中曲线b可表示使用了催化剂的能量变化情况 |
| D.图12中曲线可表示在不同压强P1、P2(P1<P2)条件下甲醇百分含量随温度变化的情况 |
下列说法正确的是()
| A.反应:2CO(g)+2NO(g) |
| B.0.1mol/L NH4C1溶液加蒸馏水稀释,溶液的pH不断减小 |
| C.铅蓄电池放电时,正极和负极均有硫酸铅生成 |
D.反应:2A(g)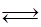 B(g)+2C(g),增大压强反应速率加快,A的转化率减小 B(g)+2C(g),增大压强反应速率加快,A的转化率减小 |
尿黑酸症是由酪氨酸在人体内非正常代谢而产生的种遗传病。其转化过程如下: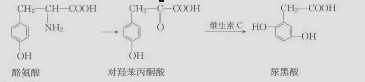
下列说法不正确的是()
| A.酪氨酸既能与盐酸反应又能与NaOH溶液反应 |
| B.对羟苯酮酸分子中有3种含氧官能团 |
| C.1mol尿黑酸最多可与含3molNaOH的溶液反应 |
| D.可用溴水鉴别对羟苯丙酮酸与尿黑酸 |
下列图示与对应的叙述一定正确的是()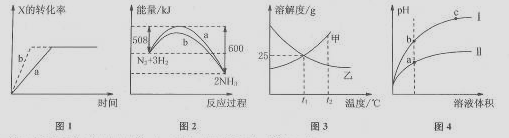
A.图1所示,反应:X(g)+2Y(g) 3Z(g),b的压强一定比a大 3Z(g),b的压强一定比a大 |
| B.图2表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 |
| C.图3所示,t1℃时质量分数均为20%的甲、乙两种溶液,升温到t2℃时,两种溶液的溶质的质量分数仍然相等 |
| D.图4所示,用水稀释pH相同的盐酸和醋酸,I表示醋酸,II表示盐酸,且溶液导电性:c>b>a |
用惰性电极电解MnO4溶液可得到MnO2,MnO2的一些性质或用途如右图,下列说法正确的是()
| A.实验室用MnO2与浓盐酸制氯气时,先将MnO2加热至高温再滴入浓盐酸 |
| B.铝置换二氧化锰中锰的反应为吸热反应 |
| C.用石墨电极电解MnSO4溶液,在阳极得到MnO2 |
| D.上述反应中二氧化锰均是氧化剂 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是()
| A.pH=13的氢氧化钠溶液,含Na+数目为0.1NA |
| B.标准状况下,22.4L乙醇中含C—H键数目为5NA |
| C.常温下,14g乙烯与2—丁烯的混合气体,含C—H键数目为2NA |
| D.反应:4Mg+10HNO3(极稀) |