元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为 )
)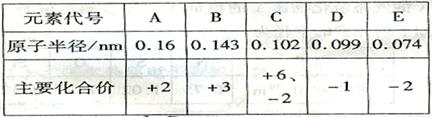
(1)B与D形成的化合物是 ;A和E形成的化合物是 。(填离子化合物或共价化合物)
(2)C的氢化物的电子式为 。
(3)B的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为: ;
(4)上述五种元素的最高价氧化物对应水化物的酸性最强的是 (填化学式);
(5)C、E形成的化合物为 、 (填化学式)
物质A有如下反应路线: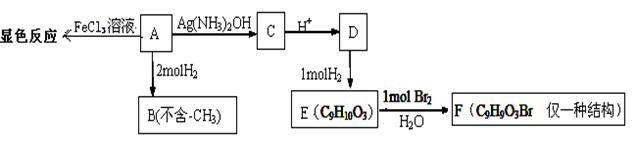
(1)1mol 物质A最多能消耗H2的物质的量为
(2)A→C的化学方程式为;
(3)H、G与B互为同分异构,且满足下列条件:①H、G与浓溴水和NaHCO3都不反应,且结构中均不含有-CH3(官能团不能同时连在同一个碳原子上)。②1molH、G 都能与2molNa反应。③H环上一氯取代只有2种,G环上一氯取代只有3种。H的结构简式为;G的一种结构简式为。
(4)已知在一定条件下R1CH=CHR2 → R1CHO+ R2CHO,A在一定条件下氧化生成羧酸X、Y。
X是芳香族化合物,Y是一种还原性的二元羧酸。
写出X在浓硫酸条件下的缩聚反应方程式。
有甲、乙、丙三种物质:


甲乙丙
(1)关于乙下列叙述正确的是
a.1mol该有机物在加热和催化剂作用下,最多能和2molNaOH反应
b.该有机物能使酸性KMnO4溶液褪色
c.该有机物的分子式为C9H11Cl
d.该有机物在一定条件下,能发生消去反应、取代反应、氧化反应和还原反应
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):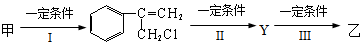
① 反应Ⅰ的反应条件是_________________________________________
②其中反应II的化学方程式是
(3)由甲出发合成丙的路线之一如下:
写出反应③的化学方程式__________________________________________________
②写出丙的结构简式_________________________
为测定某有机化合物X的结构,进行如下实验:
(1)取一定量有机物X在氧气中完全燃烧,测得生成8.8g CO2和3.6g H2O,消耗标准状况下的氧气5.6L,则X中含有种元素。
(2)用质谱仪测得A的相对分子质量为44,则X的分子式为。
(3)根据价键理论,试写出X可能的结构简式(不考虑含有 结构的物质)。
结构的物质)。
(4)X的核磁共振氢谱中出现两个不同位置的峰,则X与氢气反应的化学方程式是。
按要求完成下列问题:
①某高分子有机物 是由一种单体缩聚而成的,该单体的键线式为
是由一种单体缩聚而成的,该单体的键线式为
②将少量水杨酸(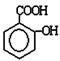 )滴入Na2CO3溶液中发生的化学方程式:______________________
)滴入Na2CO3溶液中发生的化学方程式:______________________
③CH2ClCOOCH2CH3与NaOH的水溶液共热:
④有机物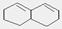 在较高温度下和Br2 按物质的量之比1:1发生加成反应的化学方程式。
在较高温度下和Br2 按物质的量之比1:1发生加成反应的化学方程式。
(1)化学式为C6H12的某烯烃的所有碳原子都在同一平面上,则该烯烃的结构简式为,其名称为;取少量该物质与氢气加成所得产物进行核磁共振分析,在核磁共振氢谱图上应该出现_____ 个峰,其面积比为(一个峰则不填)。
(2)标准状况下1.68L无色可燃气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水,得到白色沉淀质量为15.0g,若用足量碱石灰吸收燃烧产物,增重9.3g。若原气体是单一气体,它的分子式。
(3)某有机物的一氯代物分子中有两个-CH3、两个-CH2-、一个 和一个-Cl,它可能的结构有种。(本题不考虑对映异构体)
和一个-Cl,它可能的结构有种。(本题不考虑对映异构体)