如图,在一个盛有澄清石灰水的容器中有一支燃着的蜡烛,现用一只杯子将蜡烛罩住,猜想一下,杯子内会有什么现象发生 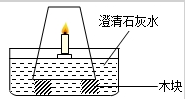
| A.蜡烛燃烧不变,液面不变 |
| B.火焰逐渐熄灭,液面下降 |
| C.蜡烛燃烧更旺,液面上升 |
| D.火焰逐渐熄灭,液面上升 |
“绿水青山就是金山银山”,下列做法与这一理念不相符的是( )
A.用布袋代替塑料袋购物
B.自带水杯出行,不用一次性纸杯
C.为增加喜庆气氛,在节日期间大量燃放烟花爆竹
D.用乙醇汽油替代部分燃油,用电动车逐步替代燃油车
将铜粉和铁粉的混合物 m g 放入烧杯中,向烧杯中不断加入FeCl3溶液,测得烧杯中剩余固体的质量与加入 FeCl3 溶液体积的关系如图所示。下列相关说法正确的是( )
[小资料]
铁和铜都能与 FeCl3溶液发生反应,反应的化学方程式为:Fe+2FeCl3=3FeCl2;Cu+2FeCl3=2FeCl2+CuCl2

A.FeCl3 与Cu 发生的化学反应属于置换反应
B.铜粉和铁粉的混合物中,铁粉的质量为(m﹣n) g
C.N 点对应的溶液中一定含有 Fe2+、Cu2+和 Cl﹣
D.当加入V1 mL FeCl3 溶液时,Cu 恰好完全反应
化学概念之间在逻辑上存在并列、交叉和包含等关系。下列各图中概念之间关系正确的是( )
A.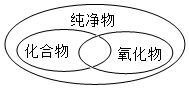
B.
C.
D.
t1℃时,将a、b两种固体物质(均不含结晶水)各25g,分别加入盛有100g水的烧杯中,充分搅拌后现象如图甲所示;升温到t2℃时,忽略水分蒸发,现象如图乙所示。图丙是a、b两种固体物质在水中的溶解度曲线。下列说法正确的是( )
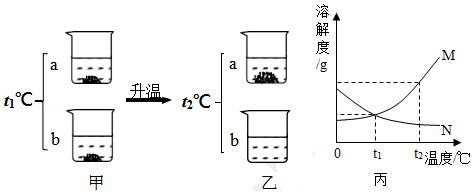
A.图甲中两烧杯内a、b溶液的溶质质量分数相等
B.图乙中烧杯内b溶液的溶质质量分数为25%
C.图丙中曲线M表示a物质的溶解度曲线
D.若a中混有少量b,可将其溶液蒸发结晶、趁热过滤以提纯a
分离与提纯是获得物质的重要方法。下列实验操作不能达到实验目的是( )
|
实验目的 |
实验操作 |
|
|
A |
除去氢氧化钠溶液中的碳酸钠 |
加入过量的石灰水,充分反应后过滤 |
|
B |
除去氮气中的氧气 |
将气体缓缓通过足量的灼热铜网 |
|
C |
除去硫酸铜溶液中的硫酸 |
加入过量的氧化铜粉末,充分反应后过滤 |
|
D |
除去银粉中的锌粉 |
加入过量的稀盐酸,充分反应后过滤、洗涤、干燥 |
A.AB.BC.CD.D