在下列①Ne、②CO2、③SiO2、④CH4、⑤Na2O2、⑥MgCl2六种物质中,请用编号填空:
其中不存在化学键的是 ,属于原子晶体的是 ,是离子化合物,且离子个数之比是2:1或1:2的是 ,只含共价键且为直线型分子的是 ,既含有离子键又有共价键的是 ,为正四面体结构的分子是 。
硫酸必须过量的目的是。
(本题共10分)
利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如下右图。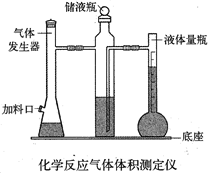
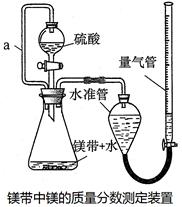
32.用离子方程式表示测定实验的反应原理。
若b为非金属元素,则以下推断正确的是_________(选填编号)。
①a一定是金属元素②d一定是金属元素③f一定是非金属元素
若f元素的原子L层电子数比M层电子数多1个,则e元素的非金属性比f元素的非金属性_________(选填“强”、“弱’’),能说明这一事实的化学方程式是__________________(任写一个)。
若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是;六种元素中,最高价氧化物对应水化物的酸性最强的是_________(填元素符号)。