下列离子方程式书写正确的是
A.电解饱和食盐水2H++2Cl¯ H2↑+Cl2↑ H2↑+Cl2↑ |
| B.向NH4HSO3溶液中滴入足量NaOH溶液:HSO3-+ OH-=SO42—+ H2O |
| C.向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2 + 2H+ = Fe2+ + 2H2O |
| D.足量AlCl3溶液与小苏打溶液混合: Al3++3HCO3-===Al(OH)3↓+3CO2↑ |
下列有关化学用语的表示方法中正确的是
A.氯元素的原子结构示意图是: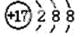 |
| B.N2的结构式:N≡N |
C.原子核内有8个中子的氧原子: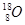 |
D.CO2的电子式是: |
下列反应过程中,同时有离子键、极性键和非极性键的断裂和形成的是
A.NH4Cl NH3↑+HCl↑ NH3↑+HCl↑ |
| B.NH3+CO2+H2O===NH4HCO3 |
| C.2Na2O2+2H2O===4NaOH+O2↑ |
| D.2NaOH+Cl2===NaCl+NaClO+H2O |
某元素原子价电子构型3d54s2,其应在
| A.第四周期ⅡA族 | B.第四周期ⅡB族 |
| C.第四周期ⅦA族 | D.第四周期ⅦB族 |
下列化合物中含有2个手性碳原子的是
A.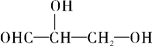 |
B. |
C.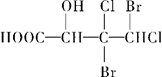 |
D. |
同学们使用的涂改液中含有很多有害的挥发性物质,二氯甲烷就是其中一种,吸入会引起慢性中毒,有关二氯甲烷的的说法正确的是
| A.含有非极性共价键 | B.键角均为109°28′ |
| C.有两种同分异构体 | D.分子属于极性分子 |