下列两个反应均为在溶液中进行的反应,试按下列要求作答:
①在表格中填出反应式中的氧化剂、还原剂,氧化产物、还原产物。
②将其改写成离子方程式;
(1) 2FeCl3 + H2S =2FeCl2 + S↓ + 2HCl
| 氧化剂: |
|
还原剂: |
|
| 氧化产物: |
|
还原产物: |
|
离子方程式为:____________________________________。
(2)MnO2 + 4HCl(浓) 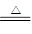 MnCl2 + 2H2O + Cl2↑
MnCl2 + 2H2O + Cl2↑
| 氧化剂: |
|
还原剂: |
|
| 氧化产物: |
|
还原产物: |
|
离子方程式为:___________________________________。
环境和材料是现在社会中两大关注的问题,请回答:
(1)造成居室污染的物质是。 A.甲醛 B.氮气 C.一氧化碳 D.二氧化碳
A.甲醛 B.氮气 C.一氧化碳 D.二氧化碳
(2)形成酸雨的原因主要是由人为排放的(填字母,下同)转化而成的。
A.SO2 B.NO2 C.CO2 D.CO
(3)造成水体富营养化的主要原因是。
A.汞(Hg)、镉(Cd) B.N、P的化合物
C.石油泄漏 D.工厂排放酸、碱、盐
(4)造成白色污染的主要原因是。
A.废塑料制品 B.废铝制易拉罐
B.废旧电池 D.生活垃圾
(5)为了治理汽车尾气的污染问题,可以在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成CO2和N2,写出该反应的化学方程:。
(6)合金是被广泛应用的金属材料,下列有关合金性质的说法正确的是。
A.合金的熔点一般比它的成分金属高
B.合金的硬度一般比它的成分金属低
C.组成合金的元素种类相同,合金的 性能就一定相同
性能就一定相同
D.合金与各成分金属相比,具有许多优良的物理、化学或机械性能
(7)塑料、合成橡胶和是常说的三大合成材料。
(8)下列条件下铁钉最容易生锈的是
A.浸泡在植物油中 B.浸泡在海水中
C.置于干燥的空气中 D.浸泡在蒸馏水中
下表是某食品包装上的说明,表中列出了部分配料。
配料中,富含维生素的是 (填序号,下同),属于调味剂的是 ,属于着色剂的是 ,属于防腐剂的是  。
。
(1)属于人体生命必需微量元素的是__________。(填”Fe”、”H”或 “Na”);
(2)乙烯经加聚反应生成的聚乙烯的结构简式是
_________________________。
(3)钢铁暴露在潮湿空气中发生电化学腐蚀的实质:钢铁表面的水膜与铁组成无数微小的______________________________。
已知某条件下,1molN2(气态)与适量H2(气态)完全反应后生成 NH3(气态),放出92.2 kJ的热量,请写出该反应的热化学方程式:
______________ __________________________________________________
__________________________________________________
现有下列四种物质:①NH4Cl、②Cl2、 ③FeCl3、④NO。其中,能够与氢氧化钙加热条件下反应生成能使湿润的红色石蕊试纸变蓝的气体的是(填序号,下同),遇到KSCN溶液能变红的是,易与空气中氧气反应的是,通常状况下呈黄绿色的是。
③FeCl3、④NO。其中,能够与氢氧化钙加热条件下反应生成能使湿润的红色石蕊试纸变蓝的气体的是(填序号,下同),遇到KSCN溶液能变红的是,易与空气中氧气反应的是,通常状况下呈黄绿色的是。