已知某有机物A的红外光谱和核磁共振氢谱图如下图所示,下列说法中不正确的是( )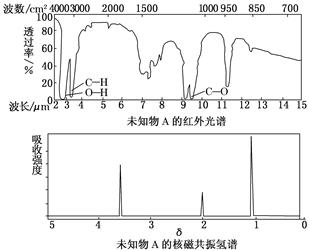
| A.由红外光谱可知,该有机物中至少有三种不同的化学键 |
| B.由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子 |
| C.仅由其核磁共振氢谱图无法得知其分子中的氢原子总数 |
| D.若A的化学式为C2H6O,则其结构简式为CH3—O—CH3 |
三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型理由的叙述,不正确的是
| A.PCl3分子中三个共价键的键长,键角都相等 |
| B.PCl3分子中的P-Cl键属于极性共价键 |
C.PCl3分子中三个共价键键能,键角均相 等 等 |
| D.PCl3是非极性分子 |
在 乙烯分子中有5个σ键、一个π键,它们分别是
乙烯分子中有5个σ键、一个π键,它们分别是
| A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键 |
| B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键 |
| C.C-H之间是sp2形成的σ键,C-C之间是未参加杂化的2p轨道形成的π键 |
| D.C-C之间是sp2形成的σ键,C-H之间是未参加杂化的2p轨道形成的π键 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
| A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| D.氨气分子是极性分子而甲烷是非极性分子。 |
下列不能形成配位键的组合是
| A.Ag+、NH3 | B.BF3、NH3 | C.Co3+、CO | D.Ag+、H+ |
下列物质中,难溶于CCl4的是
| A.碘单质 | B.水 | C.苯 | D.甲烷 |