下列化学药品与其危险化学品图形标志不一致的一组是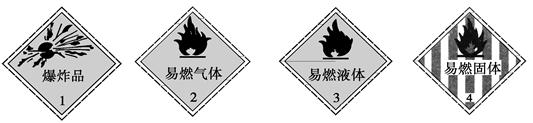
| A.烧碱——1 | B.甲烷——2 | C.酒精——3 | D.白磷——4 |
“绿色化学”提倡,设计制备物质的方案时,要从经济、环保和技术等方面考虑,以下由铜制取硝酸铜的四种方案中,比较符合“绿色化学”概念且可行的方案是
| A.Cu → Cu(NO3)2 | B.Cu → CuO →Cu(NO3)2 |
| C.Cu → CuCl2 →Cu(NO3)2 | D.Cu → CuSO4 →Cu(NO3 )2 )2 |
能证明硅酸的酸性弱于碳酸酸性的实验事实是
| A.CO2通入可溶性硅酸盐中析出硅酸沉淀 | B.CO2溶于水形成碳酸,SiO2难溶于水 |
C.高温下SiO2与碳酸盐反应生成C O2 O2 |
D.在可溶性硅酸盐中加盐酸会析出硅酸沉淀 |
在下列溶液中通入CO2至过量,原溶液一直保持澄清的是
| A.硅酸钠溶液 | B.氯化钡溶液 | C.石灰水 | D.漂白粉溶液 |
你认为减少酸雨产生的途径可采取的措施是
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫; ④在已酸化的土壤中加石灰;
⑤开发新能源
| A.①②③ | B.②③④ | C.①③⑤ | D.①④⑤ |
将盛有N2和NO2混合气体的试管倒立于水中,经过足够的时间后,试管内的气体体积缩小为原体积的一半,则原混合气体中N2与NO2的体积比是
| A.1:1 | B.1:2 | C.1:3 | D.3:1 |