有Fe2+、NO3–、Fe3+、NH4+、H+ 和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是
| A.若有l mol NO3-参加还原反应,则转移8mol e- |
| B.还原产物为NH4+ |
| C.氧化剂与还原剂的物质的量之比为8:l |
| D.若把该反应设计为原电池,则负极反应为Fe2+ -e-=Fe3+ |
已知一些金属单质的发现与其金属活动性存在着某种必然的联系,你认为下列事件发生在铁器时代之前的是:①金属铝的冶炼;②青铜器时代;③金银的使用;④戴维发现金属钠;⑤15世纪中国使用锌铸币
| A.②③⑤ | B.②③ | C.①②③ | D.①④⑤ |
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
尼泊金甲酯可在化妆品中作防腐剂。结构简式为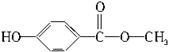
下列说法中不正确的是( )
| A.该物质属于芳香烃 |
| B.该物质的分子式为C8H8O3 |
| C.该物质能够和FeCl3反应,使溶液呈紫色 |
| D.在一定条件下,1 mol该物质最多能和2 mol NaOH反应 |
胡椒酚是植物挥发油中的一种成分。关于胡椒酚的下列说法:①该化合物属于芳香烃;②分子中至少有7个碳原子处于同一平面;③它的部分同分异构体能发生银镜反应;④1 mol该化合物最多可与2 mol Br2发生反应。其中正确的是( )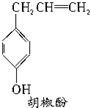
| A.①③ | B.①②④ |
| C.②③ | D.②③④ |
二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO—CH2CH2—O—CH2CH2—OH。下列有关二甘醇的叙述正确的是( )
| A.不能发生消去反应 |
| B.能发生取代反应 |
| C.能溶于水,不溶于乙醇 |
| D.符合通式CnH2nO3 |