某温度下2 L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示。下列说法正确的是( )
| |
X |
Y |
W |
| n(起始状态)/mol |
2 |
1 |
0 |
| n(平衡状态)/mol |
1 |
0.5 |
1.5 |
A.该温度下,此反应的平衡常数K=6.75
B.升高温度,若W的体积分数减小,则此反应ΔH >0
C.增大压强,正、逆反应速率均增大,平衡向正反应方向移动
D.该温度下,此反应的平衡常数表达式是K=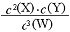
下列叙述正确的是()
A.同温同压下,相同体积的任何物质,其物质的 量一定相等 量一定相等 |
| B.相同条件下等质量O2与NH3两种气体,其体积之比为32︰17 |
| C.任何条件下,等物质的量的CH4和CO2所含的分子数一定相等 |
| D.温度和密度相同CO、N2和H2三种气体,其压强(p)关系为p(CO)=p(N2)>p(H2) |
在强酸性无色溶液中能大量共存的离子组是()
| A.Na+、K+ 、SO42-、Cl- | B.Cu2+、Na+、Cl-、CO32- |
| C.Ba2+、K+、HCO3-、NO3- | D.Mg2+、Na+、SO42-、OH- |
下列各组物质的分类都正确的是(括号里的是类别)()
| A.空气(混合物)、 Cu(单质)、H2SO4(离子化合物)、C2H5OH (非电解质) |
B.CO2 (酸性氧化物)、NH4Cl(铵盐) 、HNO3(含氧酸)、NaOH(强电解质) 、HNO3(含氧酸)、NaOH(强电解质) |
| C.H2O(非金属氧化物)、Na2O(钠盐) 、NH3 (碱)、NaCl(电解质) |
| D.CH4(有机物) 、Na2SO3(硫酸盐)、纯碱(碱)、盐酸(纯净物) |
某化学兴趣小组在实验室进行化学实验,按照图甲、乙、丙连接好线路,发现甲灯泡不亮,乙灯泡亮,丙灯泡不亮。由此得出的结论正确的是()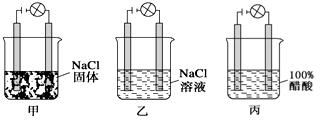
| A.醋酸是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl是弱电解质 |
| D.NaCl在水溶液中电离出了可以自由移动的离子 |
关于胶体和溶液的叙述正确的是 ()
| A.胶体带电荷,而溶液呈电中性 |
| B.胶体加入电解质可产生沉淀,而溶液不能 |
| C.溶液与胶体的本质区别是有无丁达尔效应 |
| D.带电的胶体粒子在电场作用下可定向移动,溶液中的离子在电场作用下也可定向移动 |