已知中和热的数值是57.3 kJ·mol–1。下列物质反应时,产生57.3 kJ热量的是
| A.稀HCl和稀NaOH |
| B.1.0 mol·L-1 HCl和1.0 mol·L –1 NaOH |
| C.500 mL 2.0 mol·L-1 HCl和500 mL2.0 mol·L –1 NaOH |
| D.500 mL 2.0 mol·L-1 H2SO4和500 mL 2.0 mol·L-1 Ba(OH)2 |
下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g) CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大N2的浓度时,平衡
2NH3(g),当增大N2的浓度时,平衡
向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
往平底烧瓶中放入氢氧化钡晶体和氯化铵晶体,塞紧瓶塞。在木板上滴少量水,一会儿就会发现瓶内固态物质变成液体,瓶壁变冷,小木板上因少量水冻结,而被烧瓶粘住,这时打开瓶塞,出来的气体有氨味。这是自发地发生了反应Ba(OH)2·8H20(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)下列结论中正确的是
| A.自发反应一定是放热反 | B.自发反应一定是吸热反应 |
| C.有的吸热反应也能自发进行 | D.吸热反应不能自发进行 |
如图所示是298 K时N2与H2反应过程中 ,能量变化的曲线图.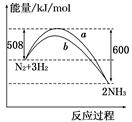
下列叙述正确的是
A.该反应的热化学方程式为:N2+3H2 2NH3 ΔH=-92 kJ/mol 2NH3 ΔH=-92 kJ/mol |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热改变 |
| D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1 |
合成氨的反应为:3H2 + N2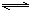 2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1),则下列关系正确的是
2NH3,其反应的速率可分别表示为v(H2)、v(N2)、v(NH3)(单位为mol·L-1·s-1),则下列关系正确的是
| A.v(H2)=v(N2)= v(NH3) | B.v(H2)=3 v(N2) |
| C.v(N2)=2 v(NH3) | D.v(NH3)=3/2v(H2) |
下列说法中正确的是
| A.反应热就是反应中放出的热量 |
| B.在101KPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
| C.由C(石墨,s)=C(金刚石,s)ΔH=+1.9kJ/mol,可知金刚石比石墨稳定 |
| D.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |