元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
| A.最外层电子数等于2的元素均为第ⅡA族元素 |
| B.在元素周期表中金属和非金属元素分界处可以找到半导体材料 |
| C.短周期元素形成离子后,最外层电子都达到了8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
下列各组物质中,不能满足“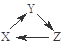 ”转化关系的一组是( )
”转化关系的一组是( )
| X |
Y |
Z |
|
| A |
Si |
SiO2 |
Na2SiO3 |
| B |
CO2 |
Na2CO3 |
NaHCO3 |
| C |
Al2O3 |
NaAlO2 |
Al(OH)3 |
| D |
Cu |
CuO |
CuSO4 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
| A.1molFeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 |
| B.标准状况下,1.12 L的HCHO所含的原子数是0.2NA |
| C.1 L0.5mol·L-1Na2CO3溶液中含有的CO32-数目为0.5NA |
| D.16.9 g 过氧化钡(BaO2)固体中阴、阳离子总数为0.3NA |
某同学在实验报告中记录下列数据,其中正确的是()
| A.用25mL量筒量取12.36mL盐酸 |
| B.用托盘天平称取8.75g食盐 |
| C.用酸式滴定管量取23.22mL高锰酸钾溶液 |
| D.用广泛pH试纸测得某溶液pH为3.5 |
下列各组物质的性质比较,正确的是()
| A.熔点:CO2<H2O<SiO2<KCl |
| B.粒子半径:K+>Na+>Mg2+>Al3+ |
| C.酸性:H3PO4>H2SO4>HClO4>H2SiO3 |
| D.稳定性:H2O<NH3<PH3<SiH4 |
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是( ) 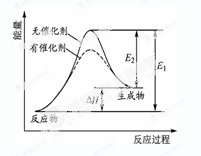
| A.该反应为放热反应 |
| B.催化剂能改变该反应的焓变 |
| C.催化剂能降低该反应的活化能 |
| D.逆反应的活化能大于正反应的活化能 |