下图中A、B、C、D四条曲线分别表示IVA、VA、VIA、VIIA族元素的气态氢化物的沸点,其中表示VIA族元素气态氢化物沸点的是曲线 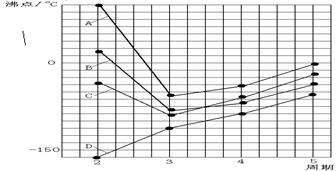
A.A B.B C.C D.D
下图是一种航天器能量储存系统原理示意图。下列说法正确的是( )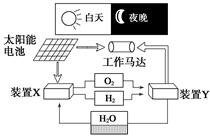
| A.该系统中只存在3种形式的能量转化 |
| B.装置Y中负极的电极反应式为O2+2H2O+4e-===4OH- |
| C.装置X能实现燃料电池的燃料和氧化剂再生 |
| D.装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
根据反应:2Ag++Cu===Cu2++2Ag,设计如右图所示原电池,下列说法错误的是( )
| A.X可以是银或石墨 |
| B.Y是硫酸铜溶液 |
| C.电子从铜电极经外电路流向X电极 |
| D.X极上的电极反应式为Ag++e-===Ag |
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为硫酸,工作时反应为:
Pb+PbO2+2H2SO4===2PbSO4+2H2O
下列结论正确的是( )
| A.Pb为正极被氧化 |
| B.SO42—只向PbO2极移动 |
| C.电解质溶液密度不断减小 |
| D.溶液的pH值不断减小 |
燃料电池是目前电池研究的热点之一。现有某课外小组自制的氢氧燃料电池,如图所示,a、b均为惰性电极。下列叙述不正确的是( )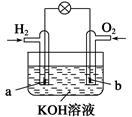
| A.a极是负极,该电极上发生氧化反应 |
| B.b极反应是O2+4OH--4e-===2H2O |
| C.总反应方程式为2H2+O2===2H2O |
| D.氢氧燃料电池是一种具有应用前景的绿色电源 |
日常所用干电池的电极分别为石墨棒(上面有铜帽)和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加入MnO2吸收H2),电极反应式可简化为:Zn-2e-===Zn2+,2NH+2e-===2NH3↑+H2↑(NH3与Zn2+能生成一种稳定的物质)。根据上述判断,下列结论正确的是( )
①锌为正极,石墨为负极 ②锌为负极,石墨为正极
③工作时,电子由石墨极经过外电路流向锌极
④长时间连续使用时,内装糊状物可能流出腐蚀用电器
| A.①③ | B.②③ | C.③④ | D.②④ |