下列关于化学反应速率的叙述,正确的是 ( )
| A.化学反应速率可用某时刻生成物的浓度表示 |
| B.在同一反应中,用反应物或生成物物质的量浓度在单位时间内的变化表示的化学反应速率的大小相等 |
| C.化学反应速率通常用单位时间内反应物浓度的减小或生成物浓度的增大来表示 |
| D.在任何反应中,反应现象在较短时间内出现,则反应速率大;反应现象在很长时间内才出现,则反应速率小 |
分析下表中各项的排布规律。有机物X是按此规律排布的第19项,下列有关X的组成、性质的说法中肯定错误的是( )
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
| CH4 |
CH2O |
CH2O2 |
CH4O |
C2H6 |
C2H4O |
C2H4O2 |
C2H6O |
①是戊酸 ②是戊醇 ③是丁酸甲酯 ④在稀硫酸中易变质 ⑤一定能与钠反应
A.②⑤ B.①③④ C.③④ D.②③⑤
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如右图。下列叙述正确的是()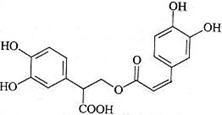
| A.迷迭香酸属于芳香烃 |
| B.1mol迷迭香酸最多能和9mol氢气发生加成反应 |
| C.迷迭香酸可以发生水解反应、取代反应和酯化反应 |
| D.1mol迷迭香酸最多能和含5mol NaOH的水溶液完全反应 |
下图表示4—溴环己烯所发生的4个不同反应。其中,产物只含有一种官能团的反应是( )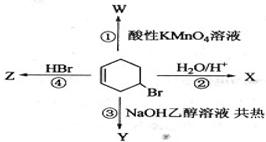
| A.①④ | B.③④ | C.②③ | D.①② |
某物质的分子式为CxHyOz,取该物质ag在足量的O2中充分燃烧后,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了bg,并且a<b,则x、y、z必须满足的关系是( )
| A.x>z | B.x=y=z | C.x=z | D.x<z |
分子式为C6H12O2且可以与碳酸氢钠溶液反应的有机物化合物(不考虑立体异构)有( )
| A.5种 | B.6种 | C.7种 | D.8种 |