在恒温时,一固定容积的容器内发生如下反应:2NO2(g)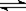 N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数( )
| A.不变 | B.增大 | C.减小 | D.无法判断 |
1 g碳与适量水蒸气反应生成CO和H2,需吸收10.94 kJ热量,此反应的热化学方程式为
| A.C+H2O=CO+H2;△H="+131.3" kJ·mol-1 |
B.C(s)+H2O(g)=CO(g)+H2( g);△H="+10.94" kJ·mol-1 g);△H="+10.94" kJ·mol-1 |
| C.C(s)+H2O(l)=CO(g)+H2(g);△H="+131.3" kJ·mol-1 |
| D.C(s)+H2O(g)=CO(g)+H2(g);△H="+131.3" kJ·mol-1 |
一定温度下,固定容积的密闭容器中进行的可逆反应:A(g)+2B(g)  C (g)+D(g),当下列物理量不再改变时,表明反应已达平衡的是
C (g)+D(g),当下列物理量不再改变时,表明反应已达平衡的是
| A.混合气体的密度不变 |
| B.A的消耗速率与D的生成速率相同 |
| C.单位时间内有1 mol A生成的同时,有1 mol C 消耗 |
| D.混合气体的相对分子质量不变 |
下列说法中,正确的是
| A.在气体反应中,增大压强能使反应物中活化分子百分数增加 |
| B.活化分子间的碰撞一定是有效碰撞 |
| C.不同化学反应需要的活化能有可能差别很大 |
| D.反应的活化能大小不会影响化学反应速率 |
对于可逆反应,当平衡向正反应方向移动时,下列说法一定正确的是
| A.反应物的转化率提高 | B.生成物的产量增加 |
| C.生成物的浓度增大 | D.生成物的百分含量增大 |
对于反应 2H2(g)+ O2(g)  2H2O(g);△H="-483.6" kJ/mol,下
2H2O(g);△H="-483.6" kJ/mol,下 列说法正确的是
列说法正确的是
| A.反应物具有的总能量高于生成物 | B.H2的燃烧热△H=-241.8kJ/mol, |
| C.破坏H-H键要放出热量 | D.升高温度重新达到平衡,平衡常数增大 |