将c(H+)=10-2mol・L-1的醋酸和盐酸分别稀释100倍,稀释后两种溶液的c(H+)分别为a和
b,则a和b的关系为 ()。
| A.a>b | B.a<b | C.a=b | D.无法判断 |
元素X的一种核素的质量数为A,中子数为N,下列推断中不正确的是
A.这种核素的符号可表示为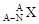 |
| B.A可以表示这种核素的近似相对原子质量 |
| C.A2+离子所含的电子数为A-N-2 |
| D.A可表示X元素的近似相对原子质量 |
在相同状况下,将下列四种混合气体:1)体积比为3∶1的NH3和N2 2)体积比为1∶1的NO和NO23)体积比为1∶1的NO2和O24)体积比为4∶3的NO和O2分别置于完全相同的试管里,并倒置于水槽中。充分反应后,液面上升的高度分别为h1 h2 h3 h4则下列关系正确的是
| A.h1> h2> h3>h4 | B.h4> h3 >h2 > h1 |
| C.h4 >h1 >h3 > h2 | D. h2 >h1 >h3 > h4 |
下列说法正确的是
| A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同。 |
| B.元素性质呈周期性变化的根本原因是核外电子排布呈周期性变化。 |
| C.元素的性质随着相对原子质量的递增而呈周期性变化。 |
| D.一切原子的原子核都是由质子和中子构成的。 |
某元素R有两种同位素,可分别表示为85R和87R,若R的近似相对原子质量为85.5则85R原子的质量分数为
| A.75% | B.25% | C.74.6% | D.64.7% |
下列物质中,既能与强酸溶液又能与强碱溶液反应的是
①Na2CO3②NaHCO3③Al2O3④Al(OH)3⑤NaHS⑥(NH4)2CO3
| A.①②③④ | B.①②③ | C.①②④ | D.②③④⑤⑥ |