下图中△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,有关说法正确的是
| A.金刚石比石墨稳定性强 |
| B.石墨变为金刚石是物理变化 |
| C.石墨变为金刚石是放热反应 |
| D.1 mol石墨的总键能比1 mol金刚石的总键能大1.9 kJ |
下列事实不能用勒夏特利原理来解释的是
| A.光照新制的氯水时,溶液中的pH值逐渐减少 |
| B.加催化剂使N2和H2在一定条件下转化为NH3 |
| C.增大压强,有利于SO2和O2反应生成SO3 |
D.在Fe3++3SCN- Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 |
已知 ;
; ,则反应
,则反应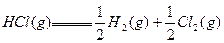 的△H为
的△H为
A. |
B.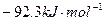 |
C.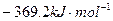 |
D.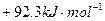 |
在密闭容器里,A与B反应生成C,其反应速率分别用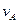 、
、 、
、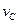 表示,已知2
表示,已知2 =3
=3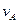 、3
、3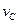 =2
=2 ,则此反应可表示为
,则此反应可表示为
| A.2A+3B="2C" | B.A+3B="2C" | C.3A+B="2C" | D.A+B="C" |
下列说法正确的是
| A.可逆反应的特征是正反应速率和逆反应速率相等 |
| B.对已达到化学平衡的反应仅改变浓度,若平衡移动,则平衡常数(K)一定不变。 |
| C.电镀时应把镀件置放电解槽的阳极。 |
| D.电解AlCl3来制取金属铝。 |
下列说法正确的是
A.NaCl固体中含有共价键 B.CO2分子中含有离子键
C.12 6C、13 6C、14 6C是碳的三种核素 D.16 8O、17 8O、18 8O含有相同的中子数