电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答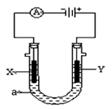
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。在X极附近观察到的实验现象是 。
②Y电极上的电极反应式为 。检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应为 。
②Y电极的材料是 ,电极反应式为 。
(说明:杂质发生的电极反应不必写出)
按要求回答下列问题:
(1) 的系统命名为 ;
的系统命名为 ;
(2)3甲基2戊烯的结构简式为 ;
(3) 的分子式为 ;
的分子式为 ;
(4)某烃的分子式为C4H4,它是合成橡胶的中间体,它有多种同分异构体。
①试写出它的一种链式结构的同分异构体的结构简式_______________________。
②它有一种同分异构体,每个碳原子均达饱和,且碳与碳的夹角相同,该分子中碳原子形成的空间构型为________________________形。
观察下列结构简式,回答下列问题:
Ⅰ、乙酸的结构简式为
(1)a的名称是__________。
(2)c的名称是________________。
Ⅱ、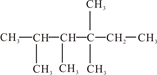
(1)有机物名称是__________________________。
(2)此有机物为烯烃加成的产物,则原来烯烃的结构可能有_______种。
写出下列化合物的名称或结构简式:
(1)结构简式为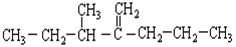 此烃名称为 。
此烃名称为 。
(2)结构简式为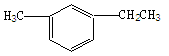 的烃可命名为 。
的烃可命名为 。 (3)2,5-二甲基-2,4-己二烯 的结构简式: 。
(3)2,5-二甲基-2,4-己二烯 的结构简式: 。
(4)结构简式为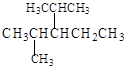 的烃可命名为: 。
的烃可命名为: 。
(6分)写出下列有机物的系统命名或结构简式
(1)2,2-二甲基-3-乙基己烷 ;
(2)CH3CH(CH3)C(CH3)2CH2CH3 ;
(3)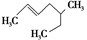 。
。
下列是一个化工生产过程的设计框图: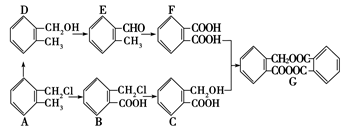
根据要求回答下列各题(填对应字母)。
(1)只含有一种官能团的物质是________。
(2)含有羧基的是________。
(3)写出G物质的分子式________。