下列表示对应化学反应的离子方程式正确的是( )
| A.用KIO3氧化酸性溶液中的KI: 5I-+IO3-+3H2O =3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热: NH4+ +OH- NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中: SO2+NH3·H2O =HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜: Ag+2H++NO3-=Ag++NO↑+H2O |
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
Fe3+有氧化性 |
实验室常用KSCN溶液检验Fe3+ |
| B |
SO2有较强的还原性 |
SO2可使酸性KMnO4溶液褪色 |
| C |
浓硫酸可干燥NO和SO2 |
NO和SO2还原性都弱 |
| D |
浓硫酸有吸水性 |
浓硫酸可用于干燥氨气 |
下图所示的实验,能达到实验目的的是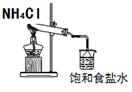

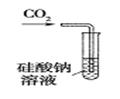
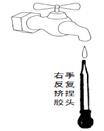
① ② ③ ④
| A.实验①制取的氨气溶解在饱和NaCl溶液 |
| B.实验②通过观察右边试管有无倒吸现象说明铁钉是否发生吸氢腐蚀 |
| C.实验③可用于证明碳的非金属性比硅强 |
| D.图④是实验室洗涤胶头滴管的操作 |
原子序数依次增大的四种短周期元素X、Y、Z、M。其中Z是金属元素,X的原子半径小于Y,Y与M同主族,Y的质子数为M的1/2。下列说法一定正确的是
| A.X与M的原子序数之差为31 |
| B.Y的离子半径小于Z的离子半径 |
| C.由X与Z组成的化合物,可与水反应放出X2 |
| D.由M与Y组成的化合物,其水化物是强酸 |
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是
| A.使酚酞变红色的溶液:Na+、Ba2+、I-、Cl- |
| B.使甲基橙变红色的溶液:Fe2+、K+、NO3-、SO42- |
| C.含有0.1 mol·L-1 Fe3+的溶液:Na+、K+、SCN-、NO |
| D.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl- |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是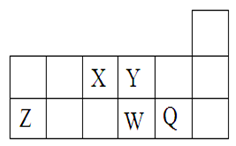
| A.离子半径的大小顺序为:r(W2—)>r(Q—)>r(Y2—)>r(Z3+) |
| B.元素W的最高价氧化物对应水化物的酸性比Q的强 |
| C.元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
| D.X、Z、W、Q四种元素的最高价氧化物对应水化物均能与强碱反应 |