现有下列短周期元素性质的数据,下列说法正确的是
| |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
| 原子半径(10-10m) |
0.74 |
1.60 |
1.52 |
1.10 |
0.99 |
1.86 |
0.75 |
0.82 |
| 最高或最低化合价 |
-2 |
+2 |
+1 |
+5;-3 |
+7;-1 |
+1 |
+5; -3 |
+3 |
A.⑧号元素为Al
B.②、③处于同一周期
C.上述八种元素最高价氧化物对应的水化物⑤号酸性最强
D.④元素的气态氢化物沸点大于⑦元素的氢化物
工业制硫酸铜不是直接用铜和浓硫酸反应,而是将粗铜(含少量银)浸入稀硫酸中,并不断从容器下部吹入细小的空气泡。有关该制备方法的叙述中,不正确的是()
| A.该方法应用了原电池工作原理 | B.该方法不产生污染大气的二氧化硫 |
| C.该方法提高了硫酸的利用率 | D.该方法提高了铜的利用率 |
下列各组离子一定能大量共存的是()
| A.含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
| B.强碱性溶液中:Na+、K+、AlO2-、CO32- |
| C.pH=7的溶液中:NH4+、Al3+、SO42-、HCO3- |
D.c(OH-)=10-13mol/L的溶液中: K+、Fe2+、Cl-、NO3- K+、Fe2+、Cl-、NO3- |
 科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列有关推测肯定不正确的是()
科技日报2007年1月30日讯:美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列有关推测肯定不正确的是()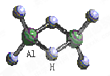

A.Al2H6跟水的反应可能是氧化还原反应,产物之一可能是氢氧化铝 |
B.Al2H6在空气中完全燃烧,产物为氧化铝和水 |
C.Al2H6分子是极性分子 |
|
| D.氢铝化合物可能成为未来的储氢材料和火箭燃料 |
下列每组物质发生所述变化克服的作用属于同种类型的是()
| A.氯化铝和干冰升华 | B.钠和硫熔化 |
| C.食盐和氯化氢溶解于水 | D.二氧化硅和二氧化硫熔化 |
NA表示阿佛加德罗常数,下列说法正确的是()
| A.0.1molFe与0.1molCl2充分反应转移电子数为0.2NA |
| B.16g甲基正离子(13CH3+)所含中子数为9NA |
| C.关于反应:C2H2(g)+2.5O2(g)= 2CO2(g)+H2O(1)+1300kJ,若CO2中有4NA 对共用电子对生成,则放出热量为1300kJ |
| D.0.lmol/L Fe2(SO4)3溶液200mL中阴离子和阳离子总数为0.1NA |