一定温度下,石灰乳悬浊液中存在下列平衡:Ca(OH)2(S)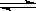 Ca2+(aq)+2OH-(aq),当向一定量的石灰乳悬浊液中加入少量生石灰时,下列说法正确的是
Ca2+(aq)+2OH-(aq),当向一定量的石灰乳悬浊液中加入少量生石灰时,下列说法正确的是
| A.溶液中Ca2+离子数目减少 | B.溶液c(Ca2+)减小 |
| C.溶液的C(OH-)增大 | D.溶液中溶质的质量分数增大 |
常温下,下列各组数据中比值为2:1的是
| A.电解熔融氯化钠,在阴极和阳极上析出产物的物质的量之比 |
| B.中和体积相同、pH相同的硫酸和盐酸消耗NaOH的物质的量之比 |
| C.1 mol·L-1氨水溶液与0.5 mol·L-1氨水溶液中c(OH-)之比 |
| D.物质的量相同的水和乙醇与足量金属钠反应产生氢气的体积之比 |
下列化学过程及其表述正确的是
| A.向NaHSO4,溶液中滴人Ba(OH)2溶液呈中性:H++SO2-4+Ba2++OH-===BaSO4↓+H2O |
| B.由水电离的c(H+)=10-13mol·L-1的溶液中,Na+、NO-3、SO42-、Cl-能大量共存 |
| C.向含有1mol KAl(SO4)2的溶液中加入Ba(OH)2溶液至沉淀质量最大时,沉淀的总物质的量为3 mol |
D.我国首创的海洋铝电池 ,采用铂网作为正极,该电池负极的电极反应式为: O2+2H2O+4e-→4OH- ,采用铂网作为正极,该电池负极的电极反应式为: O2+2H2O+4e-→4OH- |
某温度时,用惰性电极电解硝酸钠的不饱和溶液。若两极板收集到气体总体积为22.4aL时,剩余溶液恢复至原温度,析出溶质mg;若两极收集到气体总体积为33.6aL时,剩余溶液恢复至原温度,析出溶质ng。则硝酸钠在该温度时的溶解度是(气体体积均已折合为标准状况下的体积
A.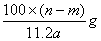 |
B. |
C.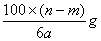 |
D.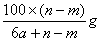 |
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2mol Cu(OH)2,恰好恢复到电解前的浓度和pH。则电解过程中转移电子的总物质的量为
| A.0.2mol | B.0.4mol | C.0.6mol | D.0.8mol |
石油原油没有固定的沸点,加热原油使其不同沸点的组分分别汽化,再分别冷凝,可分离得到汽油、煤油和沥青等物质。据此判断,石油是
| A.混合物 | B.化合物 | C.单质 | D.纯净物 |