实验室有CuO和Cu粉的混合物。请你利用给出的实验仪器及试剂,设计两种测定该样品(已称得其质量为m克)中氧化铜质量分数的方法,并填写表格中的有关内容。
实验可能用到的主要仪器:
①托盘天平 ②启普发生器 ⑧硬质玻璃管 ④泥三角 ⑤烧杯
⑥坩埚 ⑦酒精灯 ⑧玻棒 ⑨漏斗 ⑩干燥管
实验可能用到的试剂:a.锌粒 b.稀硫酸 c.氯化钠溶液 d,浓硫酸
| 实验 方法 |
实验过程中所发生反应的 化学方程式 |
实验所用仪器 (用编号表示) |
实验需直接测定的有关物理量(用文字说明) |
| 1 |
|
|
|
| 2 |
|
|
|
(1)写出实验室制乙烯的化学方程式
(2)该实验需加入碎瓷片目的是
(3)下列实验操作正确的是
A、配制乙醇与浓硫酸的混合液时,将1体积乙醇沿烧杯器壁缓缓注入3体积的浓硫酸中,并用玻璃棒不断搅拌
B、加热混合液时,应小心加热使温度缓缓上升至所需温度
C、温度计水银球的位置应伸入液面之下,而不是液面之上
D、收集乙烯气体时应用排水法收集,不能用排空气法收集
(4)在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:
① I、II、III、IV装置可盛放的试剂是
I;II;III;IV(将下列有关试剂的序号填入空格内)。
A、NaOH溶液 B、酸性KMnO4溶液 C、溴水 D、品红溶液
②能说明SO2气体存在的现象是。
③确定含有乙烯的现象是。
下图是实验室制取Cl2并以纯净、干燥的Cl2为原料进行特定反应的实验装置图: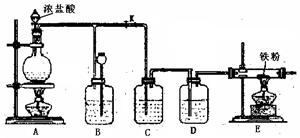
(1)写出实验室制取氯气的离子反应方程式:。
(2)C中盛装的液体是,D中盛装的液体是。
(3)实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃E处的酒精灯。E装置内盛有铁粉,写出E装置中反应的化学方程式:。 (4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是,B的作用是。
(4)E处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是,B的作用是。
(5)该装置的设计是否合理(填“是“或 “否”),如果不合理,请加以改正。
某校学生用如下图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物。
请回答下列问题:
(1)写出II中反应的化学方程式 。
(2)观察到II中的现象是 。
(3)实验开始时,关闭K2、开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。III中小试管内苯的作用是 。
(4)能说明苯与液溴发生了取代反应的现象是 。
(5)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
①用蒸馏水洗涤,振荡,分液;②用5%的NaOH溶液洗涤,振荡,分液;
③用蒸馏水洗涤,振荡,分液;④加入无水CaCl2粉末干燥;
⑤ (填操作名称)。
有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。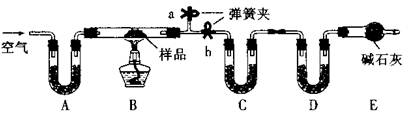
(1)实验时,B中发生反应的化学方程式为,。
(2)装置C、D中盛放的试剂分别为:
C,D(供选试剂为:浓硫酸、无水CaCl2、碱石灰)
(3)E装置中的仪器名称是,它在该实验中的主要作用是;
(4)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将(填“偏高”、“偏低”或“无影响”)
(5)反应前,在B装置中通入空气可减少实验误差,操作方法是。
实验题(12分)。已知在常用催化剂(如铂、钯)的催化下,氢气和炔烃加成生成烷烃,难于得到烯烃,但使用活性较低的林德拉催化剂[Pd/(PdO、CaCO3),其中钯附着于碳酸钙及少量氧化铅上],可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化。现有一课外活动兴趣小组利用上述原理设计了一套由如下图所示仪器组装而成的实验装置(铁架台未画出),拟由乙炔制得乙烯,并测定乙炔氢化的转化率。若用含0.020molCaC2的电石和1.60g含杂质18.7%的锌粒(杂质不与酸反应)分别与足量的X和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水VmL。试回答有关问题。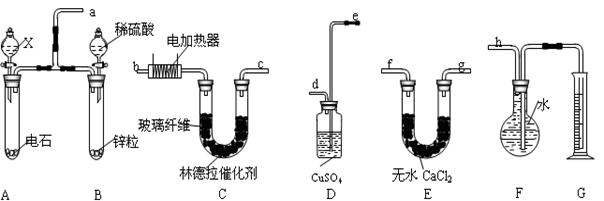 (1)所用装置的连接顺序是a、、、、、、、h(填各接口的字母)。
(1)所用装置的连接顺序是a、、、、、、、h(填各接口的字母)。
(2)写出A中所发生反应的化学方程式(有机物写结构简式):。
(3)D的作用是___________________。
(4)为减慢A中的反应速率,X应选用____________________________。
(5)F中留下的气体除含少许空气外,还有_______________________________。G所选用的量筒的容积较合理的是______________。
A.500mLB.1000mLC.2000mL
(6)若V=672mL(导管内气体体积忽略不计),则乙炔氢化的转化率为_______________。