将足量的O2 CH4 Na2O2置于一密闭容器中,用电火花反复多次引燃,完全反应后容器
内压强为零(150℃),且剩余物质溶于水无气体产生,则O2 CH4 Na2O2的物质的量之比为
| A.1∶2∶6 | B.1∶2∶3 | C.6∶3∶2 | D.3∶2∶1 |
恒温恒容下,往一真空密闭容器中通入一定量的气体A,发生如下反应:
3A(g) 2B(g)+xC(g)。达平衡后,测得容器内的压强增大了p%,A的平衡转化率为a%,则下列推断中正确的是
2B(g)+xC(g)。达平衡后,测得容器内的压强增大了p%,A的平衡转化率为a%,则下列推断中正确的是
| A.若x=2,则p>0.5a | B.若x=3,则p<0.7a |
| C.若x=4,则p= a | D.若x= 5,则p≥a |
pH=11的x、y两种碱溶液各5 mL,分别稀释至500 mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是
| A.稀释后x溶液中水的电离程度比y溶液中水电离程度小 |
| B.若x、y是一元碱,则等物质的量浓度的y的硝酸盐溶液的pH比x的硝酸盐溶液大 |
| C.若x、y都是弱碱,则a的值一定大于9 |
| D.完全中和x、y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y) |
FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、、NO的物质的量之比为1﹕1﹕1时,实际参加反应的FeS与HNO3的物质的量之比为
| A.1:7 | B.2:7 | C.1:5 | D.2:9 |
下图所示的实验过程中产生的现象与对应的图形不相符合的是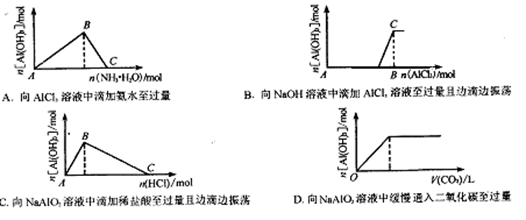
下列反应的离子方程式书写错误的是
| A.溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| B.苯酚钠溶液中通入足量CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- |
| C.铁屑溶于过量稀硝酸:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
| D.碳酸氢铵溶液与足量烧碱溶液反应:HCO3-+OH-=CO32-+H2O |