对于平衡CO2(g) CO2(aq) ΔH=-19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是 ( )
CO2(aq) ΔH=-19.75kJ/mol,为增大二氧化碳气体在水中的溶解度,应采用的方法是 ( )
| A.升温增压 | B.降温减压 | C.升温减压 | D.降温增压 |
常温下,向100 mL 0.0l mol.L-lHCl的溶液p 中逐滴加入0. 02 mol.L-lMOH溶液的过程中,其pH变化如图所示(溶液体积变化忽略不计).下列说法中正确的是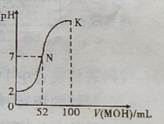
| A.MOH为一元强碱 |
| B.N点水的电离程度小于K点水的电离程度 |
| C.在K点,c(M+)>c(Cl-)>c(OH-)>c(H+) |
| D.K点对应的溶液中,有c( MOH) +c( M+)="0.02" mol.L-1 |
将物质的量浓度之比为1:2的X(g)与Y(g)在密闭容器中进行反应:X(g)+2Y(g)==32(g)+Q(s)△H>O,下列叙述一定正确的是
| A.当容器中X与Y的物质的量浓度之比满足1:2时,反应达到平衡 |
| B.达到平衡后,反应速率3v正(Y) =2v逆(z) |
| C.达到平衡时,X的转化率为25%,则平衡常数K值为1/16 |
| D.达到平衡后,升高温度,X的体积分数增大 |
下列各装置能够达到相应实验目的的是
| A.用装置甲除去乙酸乙酯中混有的少量乙酸 |
| B.用装置乙除去氯气中的少量氯化氢 |
| C.用装置丙制取无水MgCl2 |
| D.用装置丁制取乙烯 |
NA表示阿伙加德罗常数的值。下列判断正确的是
| A.常温常压下,17g氨气分子所含质子数为10NA |
| B.1mol Cl2参加反应,转移电子数一定为2NA. |
| C.常温常压下,22.4 L C02分子中含有2NA个σ键和2NA个1π键 |
| D.1 L 0. 01 mol.L-1的Na2CO3溶液中含有0.01NA个CO32- |
下列各组微粒在指定溶液中一定能大量共存的是
| A.石蕊变红色的溶液:Na+ .Mg2+ Cl—、SO2-4 |
| B.能溶解氧化铝粉末的溶液中:K+、N0-3、Cl-、NH4+ |
| C.滴加苯酚溶液显紫色的溶液:NH4,K+、Cl-、H2S |
| D.由水电离出的c ( H+)=10-12mol.L-1的溶液:Na+、K+、.NO3-、C6H5O— |