右图中的曲线是表示其他条件一定时,2NO+O2 2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( )
2NO2 △H<0 ,反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 ( ) 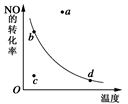
| A.a点 | B.b点 | C.c点 | D.d点 |
向存在大量Na+、Cl-的溶液中通入足量的NH3后,该溶液中还可能大量存在的离子组是()
| A.K+、Br-、CO32- | B.Al3+、H+、MnO4- |
| C.NH4+、Fe3+、SO42- | D.Ag+、Cu2+、NO3- |
阿伏加德罗常数约为6.02×1023 mol—1,下列叙述中正确的是()
| A.常温常压下,18.0 g重水(D2O)所含的电子数约为10×6.02×1023 |
| B.室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023 |
| C.标准状况下,22.4 L甲苯所含的分子数约为6.02×1023 |
| D.标准状况下,a L乙烷气体中的所含化学键数约为(a/22.4)×6.02×1023 |
下表中,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是()
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
判断 |
| A |
碳酸钠溶液可用于治疗胃病 |
Na2CO3可与盐酸反应 |
Ⅰ对,Ⅱ对,有 |
| B |
向Na2O2的水溶液中滴入酚酞变红色 |
Na2O2与水反应生成氢氧化钠 |
Ⅰ对,Ⅱ错,无 |
| C |
金属钠具有强还原性 |
高压钠灯发出透雾性强的黄光 |
Ⅰ对,Ⅱ对,有 |
| D |
过氧化钠可用于航天员的供氧剂 |
Na2O2能和CO2和H2O反应生成O2 |
Ⅰ对,Ⅱ对,有 |
下列实验方案中,能测定Na2CO3和NaHCO3混合物中NaHCO3质量分数的是()
①取a克混合物充分加热,减轻b克
②取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
③取a克混合物与足量稀硫酸充分反应,逸出气体先用浓硫酸干燥再用碱石灰吸收,碱石灰增重b克
④取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
| A.只有①②④ | B.①②③④ | C.只有①③④ | D.只有①②③ |
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:
3NF3+5H2O=2NO+HNO3+9HF。下列有关说法正确的是()
| A.NF3是氧化剂,H2O是还原剂 |
| B.若生成0.2 mol HNO3,则转移0.2 mol电子 |
| C.还原剂与氧化剂的物质的量之比为2∶1 |
| D.NF3在潮湿的空气中泄漏会产生红棕色气体 |