“卤块”的主要成分为MgCl2(含Fe2+、Fe3+、Mn2+等杂质离子),若以它为原料,按如下工艺流程图,即可制得“轻质氧化镁”。如果要求产品尽量不含杂质离子,而且成本较低,流程中所用试剂或pH值控制可参考下列附表确定。轻质氧化镁工艺流程图如下:
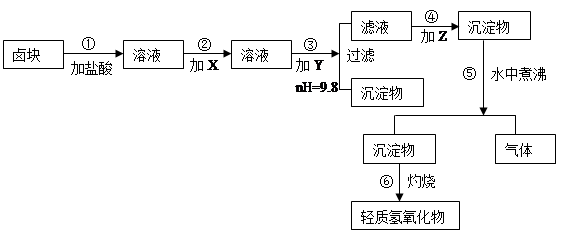
表1 化学试剂价格表
| 试剂 |
价格(元/ t ) |
| 漂液(含NaClO25.2%) H2O2(30%) NaOH(固98%) Na2CO3(固99.5%) 卤块(MgCl2,30%) |
450 2400 2100 600 310 |
表2 生成氢氧化物沉淀的值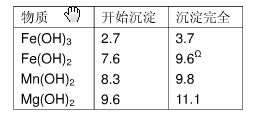
| 物质 |
开始沉淀 |
沉淀完全 |
| Fe(OH)3 Fe(OH)2 Mn(OH)2 Mg(OH)2 |
2.7 7.6 8.3 9. 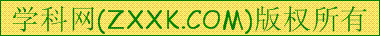 6 6 |
3.7 9.6Ω 9.8 11.1 |
Ω注:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化成为Fe3+,生成Fe(OH)3沉淀而去除之。请填写以下空白:
⑴、在步骤②加入试剂X,最佳选择应是 ,其作用是 。
⑵、在步骤③加入的试剂Y应是 ,之所以要控制pH=9.8,其目的
是 。
⑶、在步骤⑤时发生的化学反应方程式是: 。
有机物A只含有C、H、O三种元素,常用作有机合成的中间体。16.8 g该有机物经燃烧生成44.0 g CO2和14.4 g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O-H键和-C≡C-H,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1。
(1)A的分子式是 。
(2)下列物质中,一定条件下能与A发生反应的是 。
a.H2b.Na c.酸性KMnO4溶液 d.Br2
(3)A的结构简式是 。
(4)有机物B是A的同分异构体,能发生银镜反应,1 mol B最多能与2 mol H2加成。B中所有碳原子一定处于同一个平面,请写出所有符合条件的B的结构简式(不考虑立体异构) 、 。
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
(1) 贝诺酯分子式为
(2) 对乙酰氨基酚在空气易变质,原因是 。
(3) 用浓溴水区别乙酰水杨酸和对乙酰氨基酚,方案是否可行 (填“可行”或“不可行”)。
(4)写出乙酰水杨酸与足量氢氧化钠溶液反应的化学方程式 。
(5)实验室可通过两步反应,实现由乙酰水杨酸制备 ,请写出两步反应中依次所加试剂的化学式 、 。
,请写出两步反应中依次所加试剂的化学式 、 。
下图为某有机物的质谱图,测得其含碳量为76.6%,含氢量为6.4%,其余为氧元素。
(1)该有机物的分子式为_____________________________;
(2)往该有机物溶液中滴入FeCl3溶液,可以看到溶液呈紫色,可以确定该有机物的结构简式为_______;
(3)该有机物与浓溴水反应的方程式为_______________________________;
(4)往该有机物的水溶液一般呈白色浑浊状,往溶液中滴入NaOH溶液,现象是______________,反应方程式为_______________________。
在北方,常用乙二醇作内燃机的抗冻剂。某种合成乙二醇的路径如下图所示: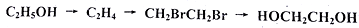
(1)按先后顺序,依次完成上图中每步反应的化学方程式:
①_______________________________________
②_______________________________________
③_______________________________________
(2)一定条件下,乙二醇可以被氧化为乙二醛,反应方程式为:______________________________
(3)CH2BrCH2Br有一同分异构体,其结构简式为:______________________________
家庭使用的天然气主要成分是甲烷,液化石油气的主要成分为丙烷。
(1)将等物质的量的甲烷和氯气混合后,在漫射光的照射下充分反应,所得产物中物质的量最大的是________(写化学式,下同),在所有生成物中,和甲烷分子一样具有正四面体结构的物质是___________;
(2)液化石油气燃烧的主要化学方程式为__________________________;现有一套以天然气为原料的灶具,欲改为烧液化石油气,需要对灶具进行改装的措施是:_______________空气进量(填“增大”或“减小”);
(3)丙烷可以认为是丙烯的加成产物,也可以认为是某块的加成产物,该炔是_________(写结构简式);
(4)丙烯跟溴起加成反应,标准状况下,11.2L丙烯可以与________gBr2完全反应。