A、B、C、D、E代表5种元素。请填空:
1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其原子核外电子的运动状态有 种。
2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,
B原子的价电子排布图为 ,C元素的原子结构示意图为 。
3)D元素的正三价离子的3d亚层为半充满,D的元素符号为 ,其基态原子的价电子排布式为 。
4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为 ,其基态原子的电子排布式为 。
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ·mol-1表示。请认真观察右图,然后回答问题。
(1)图中所示反应是_________(填“吸热”或“放热”)反应,该反应_____________(填“需要”或“不需要”)加热,该反应的△H =______________________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+ O2(g) = 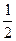 H2O(g)△H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ·
H2O(g)△H =-241.8 kJ·mol-1,该反应的活化能为167.2 kJ· mol-1,则其逆反应的活化能为____________________。
mol-1,则其逆反应的活化能为____________________。
把煤作为燃料可通过下列两种途径 :
:
途径I:C(s) +O2 (g) ==CO2(g)△H1<0①
途径II:先制成水煤气:C(s) +H2O(g) ==CO(g)+H2(g)△H2>0②
再燃烧水煤气:2CO(g)+O2 (g) ==2CO2(g)△H3<0③
2H2(g)+O2 (g) ==2H2O(g)△H4<0④
请回答下列问题:
(1) 途径I放出的热量( 填“大于”“等于”或“小于”) 途径I I放出的热量,原因是
I放出的热量,原因是
。
(2) △H1、△H2、△H3、△H4的数学关系式是。
(3)12g 炭粉在氧气中不完全燃烧生成一氧化碳,放出110.35kJ热量。其热化学方程式为
(相对原子质量C-12)。
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①分别用0.1 mol /L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
②与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快 B.H2SO4最快 C.CH3COOH最快 D. 一样快
一样快
(3)某温度下,纯水中c(H+)=2×10-7 mol/L,则此时0.02mol/LBa(OH)2溶液的pH =
(4)有四种一元酸HA、HB、HC、H D,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质
D,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质 的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,电池总反应式为:
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是___________________________;电解质溶液中H2SO4的浓度将_______ (填“变大”、“变小”或“不变”);当外电路通过1 mol电子时,理论上负极板的质量增加_______ g。
(2)在完全放电耗尽PbO2和Pb时,若按图连接,电解一段时间后,则在A电极上生成____________、B电极上生成______________,此时铅蓄电池的正负极的极性将_______________________。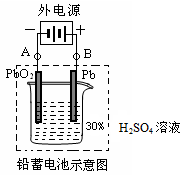
下图中每一方框中的字母代表一种反应物或生成物(部分产物未列出):
已知C是紫红色金属固体,B的浓溶液和稀溶液都是有强氧化性。
(1)A的化学式是,E化学式是;
(2)电解反应的化学(或离子)方程式是;
(3)对200ml 1mol/L的A溶液进行电解,当有0.02mol电子发生转移时,溶液的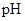 为
为
(假设溶液体积不变)。