下表是某地市场上销售的一种“加碘盐”包装上的部分文字说明。请根据此表,结合中学学过的化学知识,回答下列问题:
| 配料表 |
精制海盐、碘酸钾(KIO3) |
| 含碘量 |
20―40mg/kg |
| 储藏方法 |
密封避光、防潮 |
| 食用方法 |
烹调时待食品熟后加入碘盐 |
(1)根据物质分类中的树状分类法有关知识,在①HIO3 ②碘酸钠 ③KOH ④I2O5 ⑤NaCl五种 (填“混合物”或“化合物”或“盐”或“氧化物”)中与碘酸钾(KIO3)属于同类物质的有 (填序号)。
(2)推测出碘酸钾(KIO3)的物理性质:碘酸钾(KIO3) 溶于水(填“能”或“不能”),化学性质:碘酸钾(KIO3)在受热时 (填“分解”或“不分解”)。
(3)写出KIO3的电离方程式 。
PM2.5是连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 |
K+ |
Na+ |
NH4+ |
SO42- |
NO3- |
Cl- |
| 浓度/mol•L-1 |
4×10-6 |
6×10-6 |
2×10-5 |
4×10-5 |
3×10-5 |
2×10-5 |
根据表中数据计算PM2.5试样的pH。
(2)NOx汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
则N2和O2反应生成NO的热化学反应方程式为_________________。
(3)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下: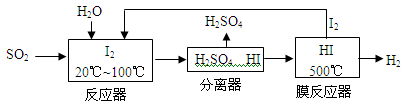
①用离子方程式表示反应器中发生的反应:_________________。
②将生成的氢气与氧气分别通入两个多孔惰性电极,KOH溶液作为电解质溶液,负极的电极反应式_________________。
(4)为了改善环境,中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
①有效“减碳”的手段之一是节能,下列制氢方法最节能的是________(填序号)。
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O(g) 2H2+O2
2H2+O2
C.太阳光催化分解水制氢
2H2O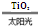 2H2↑+O2↑
2H2↑+O2↑
D天然气制氢:CH4+H2O(g) CO+3H2
CO+3H2
②CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g);ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。
CH3OH(g)+H2O(g);ΔH=-49.0 kJ·mol-1,测得CO2和CH3OH(g)浓度随时间变化如图所示。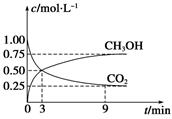
从3 min到9 min,v(H2)=_______mol·L-1·min-1。
③能说明上述反应达到平衡状态的是________(填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
④工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g)  CH3OH(g)的平衡常数。下列说法正确的是________。
CH3OH(g)的平衡常数。下列说法正确的是________。
| 温度/℃ |
0 |
100 |
200 |
300 |
400 |
| 平衡常数 |
667 |
13 |
1.9×10-2 |
2.4×10-4 |
1×10-5 |
A.该反应正反应是放热反应
B.该反应在低温下不能自发进行,高温下可自发进行
C.在T ℃时,1 L密闭容器中,投入0.1 mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5 MPa)和250 ℃,是因为此条件下,原料气转化率最高
A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题。
(1)元素D在周期表中的位置________。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)____。
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有________。用电子式表示当C、D按1:1所组成化合物的形成过程________。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:________________________________________________________________________。
(5)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:_______________________________________________________。
尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为______________________________。
(2)当氨碳比n(NH3)/ n(CO2)=4时,CO2的转化率随时间的变化关系如下图所示。
①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”、“小于”或“等于”)。
②NH3的平衡转化率为________。
③一定温度下,在一个容积不变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是(填字母,下同)。
a.容器中的压强不变b.3mol N—H键断裂的同时断裂2 molH—O键
c.c(CO2)=c(H2O)d..c(CO2)的浓度保持不变
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如下图所示。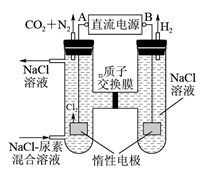
①电源的负极为________(填“A”或“B”)。
②阳极室中发生的反应依次为___________________、___________________。
③电解结束后,阴极室溶液的pH与电解前相比将________(填“增大”、“减小”或“不变”);若两极共收集到气体11.2 L(标准状况),则除去的尿素为________g(忽略气体的溶解)。
V、W、X、Y、Z是原子序数依次递减的五种常见元素。X元素是地壳中含量最多的元素,Y、Z组成气态化合物M的水溶液呈碱性,W的单质在X2中燃烧的产物可使品红溶液褪色,V是一种历史悠久,应用广泛的金属元素。请回答:
(1)Y元素在周期表中的位置是;写出X、Z两种元素组成的一种化合物的一种用途。
(2)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且属于氧化还原反应,请写出该反应的化学方程式。
(3)X、Y、Z三种元素可组成一种强酸U,M在适当条件下被U吸收生成一种盐。常温下该盐的水溶液的pH7(填“大于”、“小于”或“等于”)。
(4)W(s)+O2(g)WO2(g); H1 W(g)+O2(g)
H1 W(g)+O2(g)WO2(g); H2
H2
则 Hl(填“>”或“<”或“=”)
Hl(填“>”或“<”或“=”) H2。
H2。
(5)有人设想寻求合适的催化剂和电极材料,以Y2、Z2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式;放电时溶液中H+移向(填“正”或“负”)极。
(6)若将V金属投入到硫酸溶液中,生成了浅绿色溶液N。写出N的溶液与K2Cr2O7酸性溶液反应的离子方程式:。
已知有机物之间能发下如下反应:
下列有机化合物A~H有如下图所示的转化关系: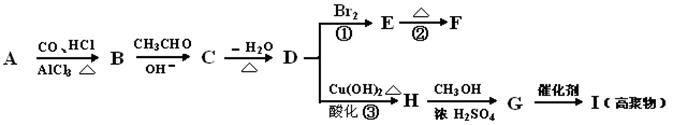
其中,化合物D的分子式为C10H10O,其苯环上的一氯代物只有两种;F的分子式为C10H8O,且所有碳原子在同一平面上。请回答下列问题:
(1)物质I的结构简式。
(2)反应①的反应类型为;反应②的条件为。化合物F的核磁共振氢谱(1H-NMR)显示有个峰。
(3)写出下列反应的化学方程式:
CH3CHO与足量HCHO反应。反应③。
(4)化合物D有多种同分异构体,满足下列条件的有种(一个碳原子上不可能两个双键)
①属于酚类;
②结构中除苯环外无其他环;
③苯环上只有两种互为对位的取代基。