A、B、C、D,E和F是六种短周期元素,它们的原子序数依次增大。 A和D,C与F为同主族元素;A的单质是最轻的气体; B元素最高价氧化物的水化物与其气态氢化物反应生成盐; E元素是地壳中含量最多的金属元素。F元素原子M层上电子数比L层少2个电子。 试完成下列填空
(1)E元素位于周期表的第 周期 族。
(2)F简单阴离子的结构示意图 。
(3)铜与B元素最高价氧化物的水化物的稀溶液反应的离子方程式为 。
(4)E的硫酸盐溶液中滴入B元素气态氢化物的水溶液,直至过量。离子方程式为 。
(15分)[选修3—物质结构与性质]钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。回答下列问题:
(1)钒在元素周期表中的位置为 ,其价层电子排布图为 。
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为 、 。
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是 对,分子的立体构型为 ;SO3气态为单分子,该分子中S原子的杂化轨道类型为 ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为 ;该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为 (填图2中字母),该分子中含有 个σ键。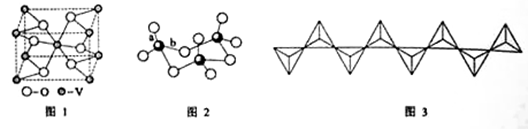
(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为 ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为 ____ 。
(15分) [选修2—化学与技术]氨气是工农业生产中重要的产品,合成氨并综合利用的某些过程如下图所示:
(1)原料气中的氢气来源于水和碳氢化合物。请写出甲烷和水在催化剂和高温条件下反应的方程式: 。
(2)在工业生产中,设备A的名称为 ,A中发生的化学反应方程式是 。
(3)上述生产中向母液通入氨气同时加入 ,可促进副产品氯化铵的析出。长期使用氯化铵会造成土壤酸化,尿素适用于各种土壤,在土壤中尿素发生水解,其水解的化学方程式是 。
(4)纯碱在生产生活中有广泛的应用,请写出任意两种用途: 。
(5)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。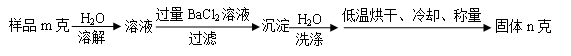
①检验沉淀是否洗涤干净的方法是_____________。
②样品中NaCl的质量分数的数学表达式为________________。
(9分) 粉煤灰中含有SiO2、Al2O3、Fe2O3等,某实验室对其进行处理的流程如图所示: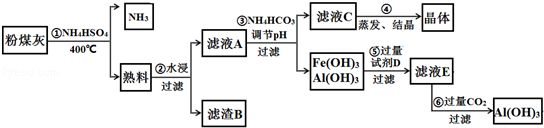
回答下列问题:
(1)第①步得到的“熟料”中可溶性的成分主要是NH4Fe(SO4)2、NH4Al(SO4)2等,写出生成NH4Fe(SO4)2的化学方程式 。在物质分类体系中,NH4Fe(SO4)2、NH4Al(SO4)2不属于 (填字母)。
a.硫酸盐 b.复盐c.强电解质d.共价化合物
(2)滤渣B的主要成分为 。
(3)已知Ksp[Fe(OH)3]=4×10-38,Ksp [Al(OH)3]=1×10-32。为实现步骤③的实验目的,应使溶液中c(Fe3+)、c(Al3+)均小于或等于1×10-5 mol•L﹣1可认为完全沉淀,则溶液A至少应调节到pH=___。
(4)实验室进行第④步操作时,所需的主要仪器是酒精灯、三脚架、 、 ,得到的晶体主要成份是 (填化学式)。
(8分) 乙苯催化脱氢制苯乙烯反应: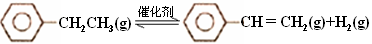
(1)已知:
| 化学键 |
C-H |
C-C |
C=C |
H-H |
| 键能/kJ·molˉ1 |
412 |
348 |
612 |
436 |
计算上述反应的△H=________ kJ·mol-1。
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数Kp=___________(用α等符号表示)。
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实 ___________。
②控制反应温度为600℃的理由是____________。
(8分) 已知:25℃时,
H2SO3 Ka1=1.5×10-2 Ka2=1.0×10-7
H2CO3 Ka1=4.4×10-7 Ka2=4.7×10-11
HNO2 Ka=5.1×10-4
HClO Ka=3.0×10-8
饱和NaClO溶液的浓度约为3 mol/L。
(1)室温下,0.1 mol/L NaClO溶液的pH 0.1 mol/L Na2SO3溶液的pH。(选填“大于”、“小于”或“等于”)。浓度均为0.1 mol/L 的Na2SO3和Na2CO3的混合溶液中,SO32–、CO32–、HSO3–、HCO3– 浓度从大到小的顺序为 。
(2)下列离子反应错误的是:_____________。
A.2HCO3-+SO2= SO32-+2CO2+ H2O
B.ClO-+CO2+ H2O=" HClO+" HCO3-
C.ClO-+SO2+ H2O=" HClO+" HSO3-
D.2ClO-+SO2+ H2O=" 2HClO+" SO32-
(3)某消毒液的有效成分为NaClO,还含有一定量的NaOH等,下列用来解释事实的方程式中不合理的是:_________。
A.该消毒液可用NaOH溶液吸收Cl2制备:Cl2 +2OH-=Cl-+ ClO-+ H2O
B.该消毒液的pH约为12:ClO-+ H2O HClO+ OH-
HClO+ OH-
C.该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2 ↑+ H2O
D.该消毒液加白醋生成HClO,可增强漂白作用: H++ ClO-= HClO
(4)25℃时,0.1 mol下列气体分别与1 L0.l mol·L-1的NaOH溶液反应,形成的溶液pH由大到小的顺序为:__________(用A、B、C、D表示)。
A.NO2B.SO2 C.SO3D.CO2