下列热化学方程式及说法正确的是( )
| A.CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) △H= —890KJ |
| B.丁烷的燃烧热是2878 kJ/mol,则: C4H10(g)+13/2O2(g)=4CO2(g)+5H2O(g)△H=" —2878kJ/mol" |
| C.2 mol氢气燃烧生成水蒸气放出484 kJ热量, 则:H2O(g)=H2(g)+1/2O2(g);△H="+242" kJ·mol-1 |
| D.CH3COOH(aq)+KOH(aq)=CH3COOK(aq)+H2O(l)△H=-akJ·mol-1,a就为中和热的值 |
甲、乙两烧杯中各盛有100 mL 3 mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲:乙=" 3" :4,则加入铝粉的质量为
| A.5.4 g | B.3.6 g | C.2.7 g | D.1.6 g |
往含等物质的量Na2CO3和NaHCO3的溶液中滴入HCl溶液,下列表示产生的气体在标准状况下的体积与加入的HCl溶液体积关系图正确的是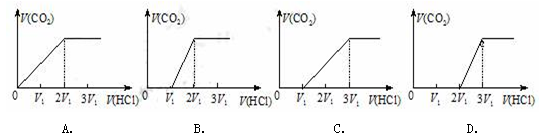
现有一块已知质量的铝镁合金,欲测定其中镁的质量分数,几位同学设计了以下三种不同的实验方案:
实验设计1:铝镁合金 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计2:铝镁合金 测定生成的气体在标准状况下的体积
测定生成的气体在标准状况下的体积
实验设计3:铝镁合金 溶液
溶液 过滤、洗涤、干燥后测定得到沉淀的质量
过滤、洗涤、干燥后测定得到沉淀的质量
则能测定出镁的质量分数的是
| A.都能 | B.都不能 |
| C.①不能,其它都能 | D.②③不能,①能 |
用一定量的铁与足量的稀H2SO4及足量的CuO制单质铜,有人设计以下两种方案:
①Fe H2
H2 Cu,②CuO
Cu,②CuO CuSO4
CuSO4 Cu。
Cu。
若实验过程中,根据一般的实验方法和实验操作规则进行操作,则两者制得单质铜的量作比较正确的是
| A.相等 | B.①多 | C.②多 | D.无法判断 |
硫代硫酸钠溶液与盐酸混合(Na2S2O3 + 2HCl ="=" 2NaCl + S↓+ SO2↑+ H2O),生成单质硫并沉淀出来。若将硫代硫酸钠溶液先与界面活性剂(不参与反应)均匀混合于烧杯中,再加入盐酸溶液并立刻搅拌,静置后无沉淀产生,得到含硫单质的胶体。下列叙述错误的是
| A.硫代硫酸钠与盐酸反应中,盐酸作还原剂 |
| B.烧杯中单质硫颗粒直径约为 10-9-10-7m |
| C.界面活性剂减缓了硫生成的速率 |
| D.用平行光照射烧杯中液体,将观察到光的“通路” |