下列反应中,在高温下不能自发进行的是
| A.MgCO3(s) ====MgO(s)+CO2(g) | B.2N2O5(g) =4NO2(g)+O2(g) |
| C.(NH4)2CO3(s) =NH3(g)+ NH4HCO3(s) | D.2CO(g) =2C(s)+O2(g) |
下列离子方程式书写正确的是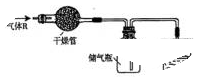
| A.金属钠投入水中:Na + H2O=Na+ + OH-+ H2↑ |
| B.铜加入稀硝酸中:3Cu + 8H+ + 2NO3-=3Cu2+ + 2NO↑+ 4H2O |
| C.向AlCl3溶液中加入过量氨水:Al3+ + 4NH3? H2O=AlO2-+ 4NH4+ + 2H2O |
| D.澄清石灰水与过量NaHCO3溶液混合:Ca2+ + OH-+HCO3-=CaCO3↓+ H2O |
在实验室里按图所示的装置来干燥、收集气体R,多余的气体R可用水吸收,则R是
| A.O2 | B.Cl2 | C.NH3 | D.CO2 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温常压下, 16gO3气体含有氧原子数为NA |
| B.标准状况下, 44.8 L四氯化碳含有的分子数为2NA |
| C.0.1mol·L-1 氯化铝溶液中含有Al3+数为0.1 NA |
| D.2.4g金属镁变为镁离子时失去的电子数为0.1NA |
以下有关原子结构及元素周期律的叙述正确的是
| A.第IA族元素铯的两种同位素137Cs比133Cs多4个质子 |
| B.同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
| C.第VIIA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |
下列有关化学用语表示正确的是
A.HCl的电子式: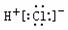 |
B.S2-的结构示意图: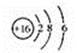 |
C.质子数为53,中子数为78的碘原子: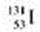 |
D.邻羟基苯甲酸的结构简式: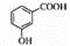 |