一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是( )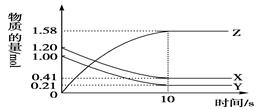
| A.反应开始到10s,用Z表示的反应速率为0.158 mol·L-1·s-1 |
| B.反应开始到10s,X的物质的量浓度减少了0.79 mol·L-1 |
| C.反应开始到10s时,Y的转化率为79.0% |
D.反应的化学方程式为:X(g)+Y (g) Z(g) Z(g) |
.关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是 ( )
| A.c(NH4+):③>① |
| B.水电离出的c(H+):②>① |
| C.①和②等体积混合后的溶液:c(H+) = c(OH-) + c(NH3·H2O) |
| D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH-) |
室温下,下列变化后的溶液pH小于8的是()
| A.pH=10的氨水稀释100倍 |
| B.pH=4的醋酸和pH=10的NaOH等体积混合 |
| C.pH=8的NaOH溶液与pH=8的Ba(OH)2等体积混合 |
| D.pH=11的NaOH溶液与pH=5的盐酸等体积混合 |
酸式盐NaHB在水溶液中,HB—的电离程度小于HB—的水解程度,下列说法正确的是( )
A.HB—水解方程式:HB-+H2O H3O+ +B2- H3O+ +B2- |
| B.溶液中离子浓度大小为:c(Na+)>c(HB-)>c(OH-) >c(H+) |
| C.NaHB的存在抑制了水的电离 |
| D.相同物质的量浓度溶液的pH值:NaHB > Na2B |
有A、B、C、D四种一元酸溶液,对它们进行的有关实验及其结果分别为:(1)在物质的量浓度相同的A、C两溶液中,都滴加几滴甲基橙时,A溶液呈黄色,C溶液呈橙色(2)B的钠盐溶液的pH值小于C的钠盐溶液pH值(3)A酸与D的盐反应生成A的盐和D酸。由此可以确定这四种酸的酸性由强到弱的正确排列顺序为 ()
A.B>C>A>D B.A>C>B>D C.D>A>C>B D.C>B>A>D
某温度下,100 mL 0.4 mol/L醋酸溶液与足量Zn粒反应生成H2的速率v(H2)=0.01mol/(L·min)。下列有关说法正确的是()
| A.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入少量CaCO3固体 |
| B.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入10 mL 0.1 mol/L醋酸溶液 |
| C.为了减缓反应速率,但又不影响生成H2的总量,可向该溶液中加入少量NaNO3溶液 |
| D.若向该溶液中加入少量醋酸钠固体,反应速率可能变成v(H2)="0.3" mol/(L·h) |