下列结论是从某同学的作业本上摘录的,其中你认为肯定正确的是
①微粒半径:S2->Cl->Cl>S ②氢化物稳定性:HF>HCl>H2S>H2Se
③还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se
⑤酸性:H2SO4>HClO4>H2SeO4 ⑥得电子能力:F>Cl>Br>I
| A.只有① | B.②④⑥ | C.①③④ | D.只有⑥ |
设NA为阿伏加德罗常数的值。下列说法中正确的是
| A.在密闭容器中加入1 mol N2和3 mol H2,充分反应生成NH3分子数为2NA |
| B.标准状况下,4.48 L N2所含的共用电子对数0.2NA |
| C.常温常压下,1 mol NaHSO4晶体中含有2NA个离子 |
| D.标准状况下,1 mol Fe与22.4 L Cl2反应转移的电子数为3NA |
下列物质的转化在给定条件下能实现的是
①SiO2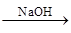 Na2SiO3
Na2SiO3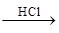 H2SiO3
H2SiO3
②Fe Fe2O3
Fe2O3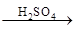 Fe2(SO4)3
Fe2(SO4)3
③BaSO4 BaCO3
BaCO3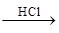 BaCl2
BaCl2
④AlCl3 Al
Al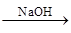 NaAlO2
NaAlO2
⑤HCHO HCOOH
HCOOH HCOOCH3
HCOOCH3
| A.①②③ | B.②③⑤ | C.③④⑤ | D.①③⑤ |
用下列实验装置和方法进行相应实验,能达到实验目的的是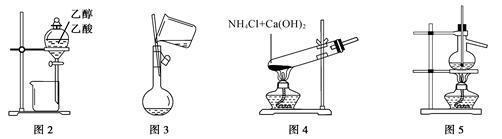
| A.用图2所示装置分离乙醇与乙酸 |
| B.用图3所示的装置向容量瓶中转移液体 |
| C.用图4所示的装置制备少量氨气 |
| D.用图5所示的装置分馏石油 |
下列有关物质的性质与应用均正确的是
| A.MgO的熔点很高,可用于制作耐高温材料 |
| B.Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒 |
| C.氨气是一种碱性气体,可用P2O5或无水CaCl2干燥 |
| D.SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力 |
下列说法不正确的是
A.水解反应NH4++H2O NH3·H2O+H+达到平衡后,升高温度平衡正向移动 NH3·H2O+H+达到平衡后,升高温度平衡正向移动 |
| B.在海轮的外壳上镶入锌块,可减缓船体的腐蚀速率 |
| C.明矾水解生成Al(OH)3胶体,可用作净水剂 |
| D.如图1所示的反应过程中A+B→X的△H<0,X→C的△H>0 |