已知可逆反应2SO2+O2 2SO3是放热反应,下列说法正确的是
2SO3是放热反应,下列说法正确的是
| A.2molSO2 与1molO2 能完全反应生成2molSO3 ,升高温度可以加快此反应的化学反应速率 |
| B.2molSO2 与1molO2不能完全反应生成2molSO3,升高温度可以加快此反应的化学反应速率 |
| C.2molSO2 与1molO2 能完全反应生成2molSO3 ,升高温度减慢此反应的化学反应速率 |
| D.2molSO2 与1molO2 不能完全反应生成2molSO3 ,升高温度减慢此反应的化学反应速率 |
室温下,用0.100mol·L﹣1 NaOH溶液分别滴定20.00mL 0.100mol·L﹣1的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是()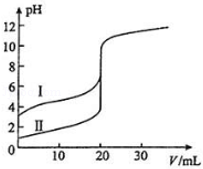
| A.Ⅱ表示的是滴定醋酸的曲线 |
| B.pH=7时,滴定醋酸消耗的V(NaOH)小于20mL |
| C.V(NaOH)=20.00mL时,两份溶液中c(Cl﹣)=c(CH3COO﹣) |
| D.V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣) |
硼酸(H3BO3)溶液中存在如下反应:
H3BO3(aq)+H2O(l) [B(OH)4]–(aq)+H+(aq).下列说法正确的是( )
[B(OH)4]–(aq)+H+(aq).下列说法正确的是( )
| A.将一滴碳酸钠溶液滴入硼酸溶液中一定能观察到有气泡产生 |
| B.将一滴醋酸溶液滴入碳酸溶液中一定能观察到有气泡产生 |
| C.等物质的量浓度的碳酸溶液和硼酸溶液比较,pH:前者>后者 |
| D.等物质的量浓度的碳酸钠溶液和醋酸钠溶液比较,pH:前者>后者 |
已知HCN的电离常数K=6.2×10﹣10。用物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,经测定溶液呈碱性.则下列关系式正确的是()
| A.c(CN﹣)>c(Na+) | B.c(CN﹣)>c(HCN) |
| C.c(HCN)+c(CN﹣)=0.2mol·L﹣1 | D.c(CN﹣)+c(OH﹣)="0.1" mol·L﹣1 |
在25℃时,向VmLpH=m的HNO3中滴加pH=n的KOH溶液10VmL时,溶液中NO3﹣的物质的量恰好等于加入的K+的物质的量,则m+n的值为( )
| A.13 | B.14 | C.15 | D.不能确定 |
现有KCl和KBr的混合物3.87g,将混合物全部溶于水,并加入过量的AgNO3溶液,充分反应后产生6.63g沉淀物,则原混合物中钾元素的质量分数为( )
| A.24.1% | B.25.9% | C.40.3% | D.48.1% |