下列物质含有的化学键类型相同的是( )
| A.NaBr和H2O | B.Na2O和Na2O2 | C.D2O和CO2 | D.NH4Cl和HCl |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是 ( )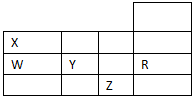
| A.常压下,五种元素的单质中,Z单质的沸点最高 |
| B.W的氢化物比X的氢化物的稳定性高 |
| C.Y、Z的阴离子电子层结构都与R原子的相同 |
| D.Y元素比W元素的非金属性强 |
以下说法中,不违背科学规律的是 ( )
①改变核外电子数可使原子与离子相互转化 ②改变核内中子数可使不同的同位素相互转化 ③改变核内质子数可使不同的元素相互转化,属于化学变化 ④改变离子的电荷数可使一种元素的阳离子转化为另一种元素的阴离子
| A.①② | B.②③ | C.③④ | D.①③ |
月球含有丰富的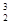 He。下列关于
He。下列关于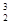 He的说法不正确的是 ( )
He的说法不正确的是 ( )
A.核外电子排布为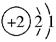 |
| B.原子核内有1个中子 |
C.与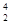 He互为同位素 He互为同位素 |
D.比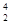 He具有相同的质子数 He具有相同的质子数 |
某固体粉末甲中可能含有K2CO3、KNO3、NaNO2、K2SO3、Na2SO4、FeO、Fe2O3中的若干种,某同学为确定该固体粉末的成分,取甲进行连续实验,实验过程及现象如下: 
该同学得出的结论正确的是
| A.根据现象1可推出该固体粉末中含有钠元素,但不含钾元素 |
| B.根据现象2可推出该固体粉末中一定含有NaNO2 |
| C.根据现象3可推出该固体粉末中一定含有Na2SO4 |
| D.根据现象4和现象5可推出该固体粉末中一定含有FeO和Fe2O3 |
25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示。下列说法正确是
| A.在上述三种盐原溶液中,水的电离度大小是NaX>NaY>NaZ |
| B.在等物质的量浓度的NaX、NaY、NaZ混合液中,离子浓度的大小关系是c(Z-)>c(Y-)>c(X-) |
| C.在上述NaX和NaY的混合液中存在c(HX)/c(X-)=c(HY)/c(Y-) |
| D.在0.2mol·L-1 NaX溶液中加入等体积0.1mol·L-1的盐酸,所得混合液中存在c(H+)+c(HX)=c(OH-)+c(Cl-) |