下列化学式只能表示一种物质的是()
| A.C4H8 | B.C4H10 | C.C3H8 | D.C2H4Cl2 |
下列物质中,在不同条件下可以发生氧化、消去、酯化反应的为( )
| A.乙醇 | B.乙醛 | C.苯酚 | D.乙酸 |
下列各组物质中,互为同系物的是( )
A.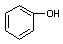 与 与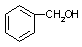 |
B.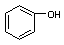 与 与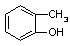 |
| C.硬脂酸与油酸 | D.甲醇与乙二醇 |
下列各组物质中,全部属于纯净物的是( )
| A.福尔马林、白酒、醋 | B.丙三醇、氯仿、乙醇钠 |
| C.苯、汽油、无水酒精 | D.甘油、冰醋酸、煤 |
某学生将一氯丙烷和NaOH溶液共热煮沸几分钟后,冷却,滴入AgNO3溶液,结果未见到白色沉淀生成,其主要原因是( )
| A.加热时间太短 | B.不应冷却后再滴入AgNO3溶液 |
| C.加AgNO3溶液后未加稀HNO3 | D.加AgNO3溶液前未用稀HNO3酸化 |