在一定温度下,下列叙述不是可逆反应A(g)+3B(g) 2C(g)达平衡时的特征的是( )
2C(g)达平衡时的特征的是( )
(1)C的生成速率与C的分解速率相等;(2)单位时间内生成amol A,同时生成3amolB;
(3)A、B、C的浓度不再变化; (4)A、B、C的压强不再变化;
(5)混合气体的总压不再变化; (6)混合气体的物质的量不再变化;
(7)单位时间内消耗amolA,同时生成3amolB;(8)A、B、C的分子数之比为1:3:2。
A (3)(8) B.(1)(6) C(2)(4) D.(2)(8)
物质的量浓度相同(0.2 mol/L)的弱酸HX与NaX溶液等体积混合后,溶液中微粒浓度关系错误的是
| A.c(Na+)+c(H+)=c(X-)+c(OH-) |
| B.c(HX)+c(X-)=c(Na+) |
| C.若混合液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) |
| D.若混合液呈碱性,则c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+) |
反应mA(固)+nB(气)  eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是
eC(气)+fD(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是
| A.达到平衡后,加入催化剂,C%不变 |
| B.该反应为放热反应 |
| C.化学方程式中m+n>e+f |
| D.达到平衡后,增加A的质量有利于平衡向右移动 |
在由水电离产生的c(H+)=1×10–14mol/L的溶液中,一定可以大量共存的离子组是
| A.NH4+、Al3+、Br–、SO42– | B.Na+、Fe2+、I–、NO3– |
| C.K+、Ba2+、Cl–、NO3– | D.K+、Na+、 I–、SO42– |
某温度下的溶液中c(H+)=10xmol/L,c(OH-)=10ymol/L。x与y的关系图所示,下列说法正确的是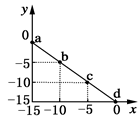
| A.该温度高于25℃ |
| B.图中a点溶液呈碱性 |
| C.该温度下,0.01 mol·L-1的HCl溶液的pH=2 |
| D.该温度下,0.01 mol·L-1的NaOH溶液的pH=12 |
蒸干下列溶液,能得到该溶质的是
| A.Na2SO3溶液 | B.KNO3溶液 | C.Fe2(SO4)3溶液 | D.AlCl3溶液 |