以下有关原子结构及元素周期律的叙述正确的是( )
| A.第 IA 族元素铯的两种同位素137Cs 比133Cs 多 4 个质子 |
| B.同周期元素(除 0 族元素外)从左到右,原子半径逐渐减小 |
| C.第 ⅦA 元素从上到下,其氢化物的稳定性逐渐增强 |
| D.同主族元素从上到下,单质的熔点逐渐降低 |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.4.0 g重水(D2O)中所含中子数为1.6 NA |
| B.1 L 2 mol·L-1 K2S溶液中S2-和HS-的总数为2 NA |
| C.2.4g金刚石与石墨的混合物中所含碳原子数为0.2 NA |
| D.50 mL 18 mol·L-1浓硫酸与足量铜反应,转移的电子数为0.9 NA |
有机物M的结构简式为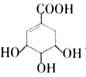 ,下列说法不正确的是
,下列说法不正确的是
| A.M的分子式为:C7H10O5 | B.M与乙酸互为同系物 |
| C.M可使溴的四氯化碳溶液褪色 | D.M在一定条件下可发生取代反应 |
900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应: ΔH=a kJ·mol—1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
ΔH=a kJ·mol—1。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| 时间/min |
0 |
10 |
20 |
30 |
40 |
| n(乙苯)/mol |
0.40 |
0.30 |
0.24 |
n2 |
n3 |
| n(苯乙烯)/mol |
0.00 |
0.10 |
n1 |
0.20 |
0.20 |
下列说法正确的是
A.反应在前20 min的平均速率为v(H2)=0.008mol·L-1·min-1
B.保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol·L-1,则a<0
C.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0%
D.相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v正>v逆
下列有关物质浓度关系的描述中,正确的是
| A.25℃时,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-7mol·L-1 |
| B.25℃时,向0.1mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性: c(Na+)>c(NH4+)>c(SO42—)>c(OH—)=c(H+) |
| C.0.1mol·L-1的NaHCO3溶液中:c(OH-)+2c(CO32-)=c(H+)+c(H2CO3) |
| D.同温下,pH相同时,溶液物质的量浓度: |
c(CH3COONa)>c(NaHCO3)>c(C6H5ONa)>c(Na2CO3)
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结 论 |
| A |
向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 |
出现白色沉淀 |
溶液X中一定含有SO42- |
| B |
等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 |
HA放出的氢气多且反应速率快 |
HB酸性比HA强 |
| C |
溴乙烷与NaOH溶液共热后,滴加AgNO3溶液 |
未出现淡黄色沉淀 |
溴乙烷未发生水解 |
| D |
向1mL1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡后再加入0.5mL有机物Y,加热 |
未出现砖红色沉淀 |
Y中不含有醛基 |