下列气态氢化物按稳定性由强到弱顺序的是( )
| A.HBr、HCl、HF | B.HF、H2O、NH3 |
| C.NH3、PH3、H2S | D.SiH4、CH4、NH3 |
下列有机物的化学用语正确的是
A.CH(CH3)3:表示正丁烷的结构简式
B.C2H4O:表示乙醇的分子式
C.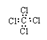 :表示四氯化碳的电子式
:表示四氯化碳的电子式
D.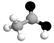 表示乙酸的球棍模型(表示C、H、O元素)
表示乙酸的球棍模型(表示C、H、O元素)
“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种.若将纳米碳均匀地分散到蒸馏水中,所形成的分散系:①是溶液 ②是胶体 ③能产生丁达尔效应 ④分散质粒子能透过滤纸 ⑤分散质粒子不能透过滤纸 ⑥静置后,会析出黑色沉淀
| A.①④⑥ | B.②③④ |
| C.②③⑤ | D.①⑤⑥ |
化学与生活密切相关,下列说法不正确的是
| A.二氧化硫可广泛用于食品的增白 |
| B.葡萄糖可用于补钙药物的合成 |
| C.聚乙烯塑料制品可用于食品的包装 |
| D.次氯酸钠溶液可用于环境的消毒杀菌 |
下列物质中属于有机物的是
①氰化钠(NaCN)②丙酮③丁炔④碳化硅(SiC) ⑤碳酸⑥CO⑦KSCN
A.①②③④⑦B.①②③C.②③D.全部都是
室内空气污染的主要来源之一是现代人的生活中使用的化工产品。如泡沫绝缘材料的办公用品、化纤地毯及书报、油漆等不同程度释放出的气体。该气体可能是
| A.甲醛 | B.甲烷 | C.一氧化碳 | D.二氧化碳 |