常温下,下列各组离子在指定的溶液中一定能大量共存的是( )
| A.水溶液:NH4+、OH-、Na+、HCO3- |
| B.0.1mol/LNaNO3溶液:H+ 、Fe2+、Cl_、SO42- |
| C.与Al反应能产生大量H2溶液:CO32—、K+、Na+、NH4+ |
| D.水溶液:OH-、S2-、Na+、CH3COO- |
下列离子方程式正确的是
A.乙酸与碳酸氢钠溶液反应:H4+HCO3- CO2↑+H2O CO2↑+H2O |
| B.醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O |
| C.苯酚溶液与Na2CO3溶液:2C6H5OH+CO32-→2C6H5O-+CO2↑+H2O |
| D.甲醛溶液与足量的银氨溶液共热 |
HCHO+4[Ag(NH3)2]+4OH- CO32-+2NH4++4Ag↓+6NH3+2H2O
CO32-+2NH4++4Ag↓+6NH3+2H2O
针对下图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的是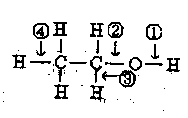
| A.与金属钠反应时,①键断裂 |
| B.与浓硫酸共热至170℃时,②、④键断裂 |
| C.与醋酸、浓硫酸共热时,②键断裂 |
| D.在Ag催化下与O2反应时,①、③键断裂 |
下列各组有机物只用一种试剂无法鉴别的是
| A.乙醇、甲苯、硝基苯 | B.苯、苯酚、己烯 |
| C.苯、甲苯、环己烷 | D.甲酸、乙醛、乙酸 |
已知丁基共有4种,可推断分子式为C5H10O2属于羧酸的同分异构体数目有
| A.3种 | B.4种 | C.5种 | D.6种 |
将0.2mol两种气态烃组成的混合气体,完全燃烧后得到6.72 L二氧化碳(标准状况下)和7.2g水,下列说法正确的是
| A.一定有甲烷 | B.一定有乙烯 | C.一定没有甲烷 | D.可能有乙烷 |