下列对各种平衡体系的叙述中,不正确的是
A.一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡:
CH3COO- +H2O CH3COOH+OH-,使得溶液中的c(OH-)>c(H+)
CH3COOH+OH-,使得溶液中的c(OH-)>c(H+)
B某温度下,容积一定的密闭容器中进行可逆反应,X(g) +Y(g) 2Z(g)+W(s)
2Z(g)+W(s) 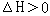 平衡后,升高温度,c(Z)增大
平衡后,升高温度,c(Z)增大
C.常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡正向移动
D.在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动
下列物质的转化在给定条件下能实现的是
① SO2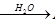 H2SO3
H2SO3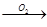 H2SO4② NH3
H2SO4② NH3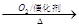 NO2
NO2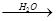 HNO3
HNO3
③ CaCl2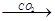 CaCO3
CaCO3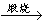 CaO④ NaAlO2(aq)
CaO④ NaAlO2(aq)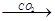 Al(OH)3
Al(OH)3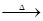 Al2O3
Al2O3
| A.②③ | B.①④ | C.②④ | D.③④ |
下列离子方程式表达正确的是
A.硫化钠水溶液呈碱性的原因:S2-+2H2O HS-+2OH-, HS-+2OH-, |
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液使SO 恰好完全沉淀: 恰好完全沉淀:2Ba2++4OH-+Al3++2 SO42-===2BaSO4↓+AlO 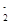 +2H2O +2H2O |
| C.氧化亚铁溶于稀硝酸中:FeO+2H+===Fe2++2H2O |
D.用惰性电极电解NaCl溶液:2Na++2Cl-+2H2O 2 NaOH+H2↑+Cl 2↑ 2 NaOH+H2↑+Cl 2↑ |
用下列实验装置完成对应的实验,能达到实验目的的是
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。五种元素核电荷数之和为54,最外层电子数之和为20。W、Z是同主族元素,Z的核电荷数是W的2倍。工业上一般通过电解氧化物的方法获得Y单质。则下列说法不正确的是
| A.原子半径:X>Y>Q>W |
| B.X、Y和W三种元素形成化合物的水溶液呈碱性 |
| C.W的氢化物的稳定性比Z强 |
| D.Q和W可形成原子个数比为1∶1和2∶1的化合物 |
下列有关物质的性质或应用的说法中正确的是
| A.石油的催化裂化及裂解可以得到较多的轻质油和气态烯烃 |
| B.Si是一种非金属主族元素,其氧化物可用于制作计算机芯片 |
| C.Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物 |
| D.蛋白质溶液中加入浓的硫酸钠溶液,有沉淀析出,这种作用称为变性。 |