下列实验装置(固定装置略去)和操作正确的是( )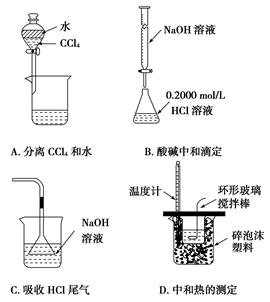
在15.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成25.4g沉淀,则下列表示气体X组成的选项中合理的是
| A.0.3 mol NO2、0.1 mol NO | B.0.3 mol NO、0.1 mol NO2 |
| C.0.6 mol NO | D.0.3 mol NO2 |
下列根据实验操作和现象所得出的结论正确的是
| 选项 |
实验操作 |
实验现象 |
结论 |
| A |
向两份蛋白质溶液中分别滴加饱和NaCl 溶液和CuSO4溶液 |
均有固体析出 |
蛋白质均发生变性 |
| B |
向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液 |
出现白色沉淀 |
溶液X 中一定含有SO42- |
| C |
用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中 |
出现白色沉淀 |
H2CO3的酸性比H2SiO3的酸性强 |
| D |
向浓度均为0. 1 mol·L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3溶液 |
出现黄色沉淀 |
Ksp(AgCl)>Ksp(AgI) |
原电池发生的反应是可自发进行的氧化还原反应,CO/O2燃料电池以熔融状态的碳酸盐为电解质,下列说法正确的是
| A.CO在正极通入 |
| B.CO32— 在电池内部向正极移动 |
| C.当有22.4LCO参加反应时电路中有2mol电子发生转移 |
| D.该电池电解质在固态时,电池无法工作 |
下列反应的离子方程式不正确的是
| A.碳酸氢钙溶液加入过量的氢氧化钙溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B.等物质的量的NH4HCO3与NaOH在溶液中反应:NH4++OH-=NH3·H2O |
| C.在含有Mn2+的溶液中加入HNO3酸化,再加入PbO2,反应体系显紫红色:5PbO2 + 2Mn2+ + 4H+ = 5Pb2+ + 2MnO4— + 2H2O |
| D.等体积同浓度NaHSO4、Ba(OH)2两溶液混合:H++SO42—+Ba2++OH—=BaSO4↓+H2O |
化学是以实验为基础的学科,下列有关实验的描述正确的是
| A.向两支分别装有碳酸钠和碳酸氢钠固体的试管中各加几滴水,前者温度降低,后者温度升高 |
| B.向100mL容量瓶中加入4.0gNaOH固体,然后加水到刻度线,配制1.0mol/L的NaOH溶液 |
| C.向酸性重铬酸钾溶液中加NaOH,溶液颜色由橙色慢慢变为黄色 |
| D.如图所示,随着空气的通入,试管内液面会慢慢上升至充满整支试管,而后液面又下降。 |