对实验Ⅰ~Ⅳ的实验现象预测正确的是(双选)( )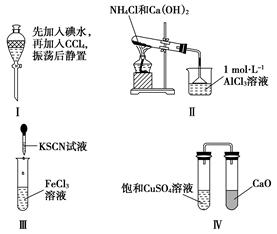
| A.实验Ⅰ:液体分层,下层呈无色 |
| B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解 |
| C.实验Ⅲ:试管中溶液颜色变为红色 |
| D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
一定温度下,向饱和NaOH溶液中投入一小块金属钠,充分反应后恢复到原来的温度。下列叙述中不合理的是
| A.NaOH溶液浓度增大,并放出H2 |
| B.溶液中NaOH的质量分数不变,有H2放出 |
| C.溶液的质量减小,有H2放出 |
| D.钠浮于液面,到处游动,发出“嘶嘶”的响声 |
Al、Fe、Cu都是重要的金属元素。下列说法正确的是
| A.三者对应的氧化物均为碱性氧化物 |
| B.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| C.三者的单质放置在空气中均只生成氧化物 |
| D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al |
下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是
①NaHCO3②(NH4)2SO3③Al2O3④Al(OH)3⑤Al
| A.全部 | B.只有①③④⑤ | C.只有③④⑤ | D.只有②③④⑤ |
能正确表示下列反应的离子方程式是
A.氢氧化亚铁溶于稀硝酸中:Fe(OH)2 + 2H+=Fe2+ + 2H2O |
B.三氧化二铁溶于氢碘酸: Fe2O3 + 6H+ = 2Fe3+ + 3H2O Fe2O3 + 6H+ = 2Fe3+ + 3H2O |
C.铝与氢氧化钠溶液反应:2Al +2OH- =" 2" AlO2 - + H2↑ |
D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3- = 3Fe3++NO↑+2H2O |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是
| A.标准状况下,22.4LNO与CO2的混合气体中含有O原子数为3NA |
| B.0.1mol NH3溶于足量水中(不考虑氨气挥发),溶液中N原子的数目为0.1NA |
| C.0.1molN2与足量的H2反应,转移的电子数是0.6NA |
| D.58.5 g的NaCl固体中含有NA个氯化钠分子 |