Fe(NO3)2溶液呈浅绿色,其中存在下列平衡:Fe2++2H2O Fe(OH)2+2H+,往该溶液中逐滴加入盐酸,发生的变化是(双选)( )
Fe(OH)2+2H+,往该溶液中逐滴加入盐酸,发生的变化是(双选)( )
| A.平衡向逆反应方向移动 |
| B.平衡向正反应方向移动 |
| C.溶液颜色由浅绿色变为黄色 |
| D.溶液颜色由浅绿色变为深绿色 |
下列除去杂质的操作方法正确的是()
| A.NO中有少量的NO2:用水洗涤后再干燥 |
| B.食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干 |
| C.N2中有少量的O2:通过足量灼热的氧化铜 |
| D.硝酸中溶有少量NO2:可向硝酸中加入少量水,使NO2与水反应生成硝酸 |
下列选项中,有关实验操作、现象和结论都正确的是()
| 实验操作 |
现象 |
结论 |
|
| A |
将过量的CO2通入CaCl2溶液中 |
无白色沉淀出现 |
生成的Ca(HCO3)2可溶于水 |
| B |
常温下将Al片插入浓硫酸中 |
无明显现象 |
Al片和浓硫酸不反应 |
| C |
将铜片放入过量的稀硝酸中 |
生成无色气体,后观察到红棕色 |
NO遇氧气反应生成红棕色的NO2 |
| D |
将SO2通入溴水中 |
溶液褪色 |
SO2具有漂白性 |
下列物质转化在给定条件下能实现的是()
①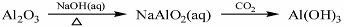
② 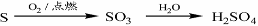
③ 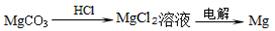
④ 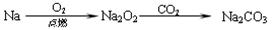
| A.①③ | B.③④ | C.②④ | D.①④ |
设NA为阿伏加德罗常数的值,下列说法正确的是()
| A.2.0gH218O与D2O的混合物中所含中子数为NA |
| B.1mol Na2O2固体中含离子总数为4 NA |
| C.标准状况下,22.4 LSO3含有NA个分子 |
| D.50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
下列有关能量的叙述错误的是()
| A.应用盖斯定律可以计算某些难以直接测定的反应热 |
| B.化学键的断裂和形成是化学反应中发生能量变化的主要原因 |
| C.HCl(aq)和NaOH(aq)反应的中和热为57.3kJ/mol,则CH3COOH(aq)和NaOH(aq)完全反应生成1mol H2O(l)时,放出的热量为57.3kJ |
| D.CO(g)的燃烧热是283.0 kJ/mol,则反应2CO2(g)=2CO(g)+O2(g)的反应热△H="+566.0" kJ/mol |