氰化物有剧毒,在碱性条件下可用如下方法进行处理: 。下列判断错误的是
。下列判断错误的是
A.上述反应中的氧化剂是 |
B.还原性: > > |
C.当有0.2 生成时,溶液中阴离子的物质的量增加1 生成时,溶液中阴离子的物质的量增加1 |
D.经测定 的水溶液呈碱性,说明 的水溶液呈碱性,说明 促进了水的电离 促进了水的电离 |
目前冰箱中使用的致冷剂是氟里昂(二氯二氟甲烷),其同分异构体有
| A.不存在同分异构体 | B.2种 | C.3种 | D.4种 |
下列各物质中,不能发生水解反应的是
| A.果糖 | B.油脂 | C.纤维素 | D.酶 |
下列物质中属于合成纤维的是
| A.人造丝 | B.蚕丝 | C.腈纶 | D.羊毛绒 |
己知维生素A的结构简式可写为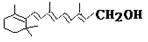 式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是
式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是
A、维生素A的分子式为C20H32O
B、维生素A能使溴的四氯化碳溶液褪色
C、1mol该有机物能跟1mol金属Na反应
D、1mol维生素A 在催化剂作用下最多可与7molH2发生加成反应
下列属于取代反应的是
| A.光照射甲烷与氯气的混合气体 | |
| B.乙烯通入溴水中 | |
| C.在镍做催化剂的条件下,苯与氢气反应 |
D.苯在浓硫酸的作用下,与浓硝酸反应 |