下列实验操作中正确的是
| A.制取溴苯:将铁屑、溴水、苯混合加热 |
| B.实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 |
| C.鉴别甲苯和苯:向甲苯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 |
| D.检验卤代烃中的卤原子:加入NaOH溶液共热,然后加入稀硝酸至溶液呈酸性,再加AgNO3 溶液,观察沉淀的颜色 |
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1 mol,下列说法一定正确的是
| A.b="2" |
| B.反应中转移的电子数一定为2NA |
| C.容器中一定没有残余的CO2和水蒸气 |
| D.a:b≥1 |
铁和稀硫酸在敞口容器中进行反应: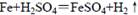 ,下列叙述中不正确的是
,下列叙述中不正确的是
A.该反应的反应过程与能量关系可以用下图表示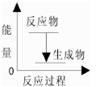 |
| B.若将该反应设计成原电池,当正极产生22.4L气体时,有56g铁溶解 |
| C.若将该反应设计成原电池,溶液中SO42-向Fe电极移动 |
| D.若将该反应设计成原电池,负极发生的反应是:Fe -2e =Fe2+ |
下列实验操作及结论正确的是
| A.使湿润的红色石蕊试纸褪色的气体一定是SO2 |
| B.量取8.58mL蒸馏水应选用10mL的量筒,而不能选用50mL的量筒 |
| C.检验氯代烃中含氯的方法是:向氯代烃中加入碱溶液,加热后先用稀硫酸酸化,再加入AgNO3溶液进行检验 |
| D.可用石墨作电极电解MgSO4和CuSO4的混合溶液,确定Mg和Cu的金属活动性强弱 |
下列关系正确的是
| A.将等物质的量的H2CO3和KHCO3溶于水配成的溶液中: 2c(K+)= c(H2CO3)+c(HCO3-) |
B.向CH3COONa溶液里加入适量的NaOH固体后得到的混合溶液中: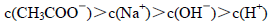 |
C.向0.10 mol·L-1 NH4HSO4溶液中滴加适量的NaOH溶液至溶液呈中性,该中性溶液中: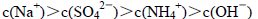 |
| D.向NaCN溶液中滴加适量的稀盐酸使溶液呈中性,该中性溶液中: |
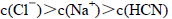
下列变化的离子方程式书写正确的是
A.将少量AgNO3溶液滴入氨水中: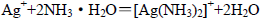 |
B.将少量SO2通入NaClO溶液中: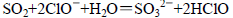 |
C.澄清石灰水与稀硝酸反应: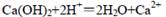 |
D.水玻璃长时间放置在空气中: |