A.A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大。第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请用对应的元素符号或化学式填空: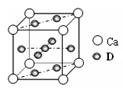
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)A的最高价氧化物对应的水化物分子中其中心原子采取 杂化。
(3)与A、B形成的阴离子(AB—)互为等电子体的分子有 。
(4)基态D原子的核外电子排布式为 ,右图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比为 。
(5)向D的高价态硫酸盐溶液中逐滴滴加B的氢化物水溶液至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液。写出此蓝色沉淀溶解的离子方程式: 。
[化学——选修物质结构与性质]碳元素在生产生活中具有非常重要的作用,在新物质的制备中也发挥了举足轻重的作用。碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图: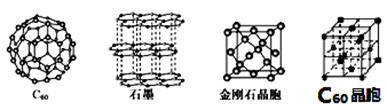
(1)与碳同周期,且基态原子的核外未成对电子数与碳相等的元素,其基态原子的电子排布式为______。
(2)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为____________。
(3)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。常温条件下丙烯是气态,而相对分子质量比丙烯小的甲醇,常温条件下却呈液态,出现这种现象的原因是______________。
(4)C60属于________晶体,C60晶体内含有的微粒间作用有_________________。
(5)金刚石晶胞含有________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=__________a,列式表示碳原子在晶胞中的空间占有率________(不要求计算结果)。
某溶液仅含下表中的某些离子,且各种离子的物质的量浓度相等,均为0.1 mol/L(此数值忽略水的电离及离子的水解)。
| 阳离子 |
K+Ag+Mg2+Cu2+Al3+NH4+ |
| 阴离子 |
Cl-CO32- NO3- SO42-I- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.取该无色溶液5 mL,滴加一滴氨水有沉淀生成,且离子种类增加。
Ⅱ.用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察,无紫色火焰。
Ⅲ.另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色。
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成。
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是________________。
(2)Ⅲ中加入盐酸生成无色气体的离子方程式是________________。
(3)甲同学最终确定原溶液中所含阳离子有_______,阴离子有______;并据此推测原溶液应该呈______性,原因是________________(用离子方程式说明)。
(4)另取100 mL原溶液,加入足量的NaOH溶液,此过程中涉及的离子方程式为__________。充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体质量为________g。
将由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水,充分反应后得到12.6g白色沉淀,向所得的浊液中逐滴加入3mol/L的盐酸,生成沉淀的质量与加入盐酸的体积的关系如图所示: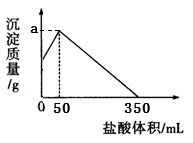
根据题意回答下列问题:
(1)写出将NaOH、AlCl3、MgCl2溶于水时发生反应的离子方程式: ___________
(2)a的值为__________
(3)求出原混合物各成分的物质的量(要求写出计算过程)
(1)近年来,我国用电弧法合成的碳纳米管中常伴有大量碳纳米颗粒(杂质),这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
C+ K2Cr2O7+ — CO2↑+ K2SO4 + Cr2(SO4)3+ H2O
①完成并配平上述化学方程式。
②在上述方程式上用单线桥标出该反应电子转移的方向与数目。
(2)高温时,用CO还原MgSO4可制备高纯MgO。750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是 。
(3)向FeCl2和FeCl3混合溶液中加入适量KOH,高速搅拌下加入油脂,过滤后干燥得到一类特殊的磁流体材料,其化学式通式为KxFeO2(其组成可理解为aK2O·bFeO·cFe2O3)。
①若x的平均值为1.3,a:b:c=_____________
②若x为1.4,请写出该磁流体在稀硫酸条件下与足量的KI溶液反应的化学方程式:_________。
(4)Fe3O4溶于稀HNO3的离子方程式:_____________。
(15分)化合物X是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成: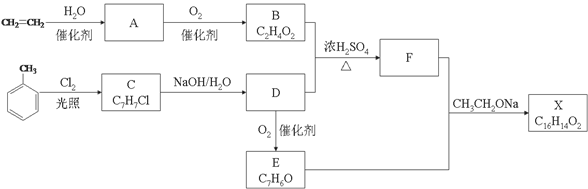
已知:RX ROH;RCHO+CH3COOR’
ROH;RCHO+CH3COOR’  RCH=CHCOOR’
RCH=CHCOOR’
请回答:
(1)E中官能团的名称是 。
(2)B+D→F的化学方程式 。
(3)X的结构简式 。
(4)对于化合物X,下列说法正确的是 。
| A.能发生水解反应 | B.不与浓硝酸发生取代反应 |
| C.能使Br2/CCl4溶液褪色 | D.能发生银镜反应 |
(5)下列化合物中属于F的同分异构体的是 。