某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如右图所示。由图中数据分析,该反应的化学方程式为_______ _______________________。
反应开始至2min,Z的平均反应速率为____ ________________。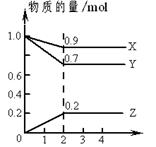
氢氧化亚铁与氢氧化铁都是铁的氢氧化物,它们有什么异同?
对下列物质按不同的分类方法进行分类。
Al2O3、Al、AlCl3、Al(OH)3、Fe2O3、FeO、Fe3O4、CaO、CuO、Fe、Cu、Ca、FeSO4、Fe2(SO4)3、Fe(OH)2、Fe(OH)3、Ca(OH)2、Cu(OH)2、CuSO4、CuCl2
将甲烷、氧气、过氧化钠放入密闭容器中,在150℃条件下用电火花引发反应后,3种物质都恰好完全反应,容器中的压强为零。则原混合物中3种物质的质量之比为___________,反应后容器中的物质是___________。
锌酸(H2ZnO2)盐不同于铝酸(H3AlO3)盐,锌酸盐稳定存在,如锌酸钠(Na2ZnO2)铝酸盐则不稳定,极易转化为偏铝酸盐,如铝酸对应的盐是偏铝酸钠(NaAlO2),而非铝酸钠(Na3AlO3)。
(1)ZnO类似于Al2O3,也是两性氧化物,试完成:
①Al2O3与NaOH(aq)的反应:____________________;
②ZnO与NaOH(aq)的反应:____________________。
(2)Zn(OH)2类似Al(OH)3,也是两性氢氧化物,试完成:
①Al(OH)3与NaOH(aq)的反应:____________________;
②Zn(OH)2与NaOH(aq)的反应:____________________。
(3)以上4个反应中,有没有氧化还原反应?若有,指出氧化剂和还原剂;若没有,说明理由。
(4)以上4个反应是不是离子反应?若是,请写出反应的离子方程式;若不是,请说明理由。
编号为A、B、C、D的4支试管,分别盛NaHSO4、NaHCO3、BaCl2、Na2CO3中的一种,但不知每支试管中究竟是何种试剂。把A分别加入到B、C、D中,有下表所列现象,试确定A、B、C、D分别是什么物质,并写出A与B、B与C反应的离子方程式。
| 反应 |
反应现象 |
| A+B |
产生无色气体 |
| A+C |
无明显现象 |
| A+D |
只产生白色沉淀 |
A______________,B______________,C______________,D______________。
A与B:__________________________________;
B与C:_______________________________。