乙醇燃料电池中采用磺酸类质子溶剂,在200℃左右时供电,电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意如图。下列说法中,正确的是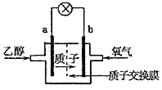
| A.电池工作时,H+向电池的负极迁移 |
| B.电池工作时,电流由a极沿导线流向b极 |
| C.a极上发生的电极反应是:C2H5OH+3H2O+12e-=2CO2+12H+ |
| D.b极上发生的电极反应是:4H++O2+4e-=2H2O |
金属Cu和一定浓度的HNO3反应:生成NO、NO2、N2O4,生成的气体恰好与11.2L O2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳在加热时反应,所产生的CO2的量
| A.小于0.5 mol | B.等于0.5 mol | C.大于0.5mol | D.无法确定 |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+7种离子中的几种.现取该溶液进行实验,得到如下现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气体冒出;②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。据此可以推断,该溶液中肯定不存在的离子是
| A.Al3+、Na+、SO32-、I- | B.Mg2+、Na+、CO32-、Br- |
| C.Al3+、Mg2+、I-、SO32- | D.Al3+、CO32-、Br-、SO32- |
下列有关离子方程式,正确的是
| A.稀硝酸和过量的铁屑反应:Fe+4H++ NO3-=Fe3++NO↑+2H2O |
B.NH4HCO3溶液与足量的NaOH溶液混合加热:NH4++HCO3-+2OH- NH3+CO32-+2H2O NH3+CO32-+2H2O |
C.碳酸氢钠溶液水解的离子方程式:HCO3-+H2O CO32-+H3O+ CO32-+H3O+ |
| D.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B.常温常压下,0.1mol铁在0.1molC12中充分燃烧,转移的电子数为0.3NA |
| C.0.1mol/L的K2CO3溶液中CO32-数小于0.1NA |
D.0.5mol雄黄(As4S4,结构如图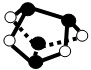 )含有NA个S—S键 )含有NA个S—S键 |
下列有机物的说法正确的是: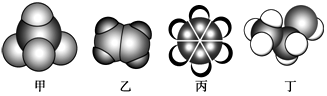
| A.C5H12有2种同分异构体 |
| B.C4H10O属于醇的结构有5种 |
| C.甲、丙分别是CH4、苯的比例模型,乙能发生加成反应,丁在一定条件下能转化为乙 |
| D.甲、乙能发生氧化反应,丙、丁不能发生氧化反应 |